Guldoxid (III) (Au2O3) struktur, egenskaper, nomenklatur och användningsområden
den guldoxid (III) är en oorganisk förening vars kemiska formel är Au2O3. Teoretiskt kan man förvänta sig att dess natur är av kovalent typ. Närvaron av en viss jonisk karaktär i dess fasta substans kan emellertid inte kasseras helt och hållet; eller vad som är samma, antar frånvaron av Au kationen3+ bredvid anjonen O2-.
Det kan tyckas motsägelsefullt att guld, som ädelmetall, kan rosta. Under normala förhållanden kan bitar av guld (som stjärnorna i bilden nedan) inte oxideras genom kontakt med syre i atmosfären; emellertid, när det bestrålas med ultraviolett strålning i närvaro av ozon, OR3, bilden är annorlunda.

Om guldstjärnorna utsattes för dessa förhållanden skulle de bli en rödbrun, karakteristisk för Au2O3.
Andra metoder för att erhålla denna oxid skulle innebära kemisk behandling av nämnda stjärnor; till exempel omvandlar guldmassan till dess respektive klorid, AuCl3.
Efter till AuCl3, och resten av möjliga guldsalter bildade, ett starkt basiskt medium tillsättes; och med detta får du den hydrerade oxiden eller hydroxiden, Au (OH)3. Slutligen dehydreras denna sista förening för att erhålla Au2O3.
index
- 1 Struktur av guldoxid (III)
- 1.1 Elektroniska aspekter
- 1,2 hydrerar
- 2 egenskaper
- 2.1 Fysisk utseende
- 2,2 molekylmassa
- 2,3 Täthet
- 2.4 Smältpunkt
- 2,5 Stabilitet
- 2.6 Löslighet
- 3 nomenklaturen
- 4 användningsområden
- 4.1 Färg av glasögon
- 4.2 Syntes av aurat och fullminderande guld
- 4.3 Hantering av självmonterade monolager
- 5 referenser
Struktur av guldoxid (III)
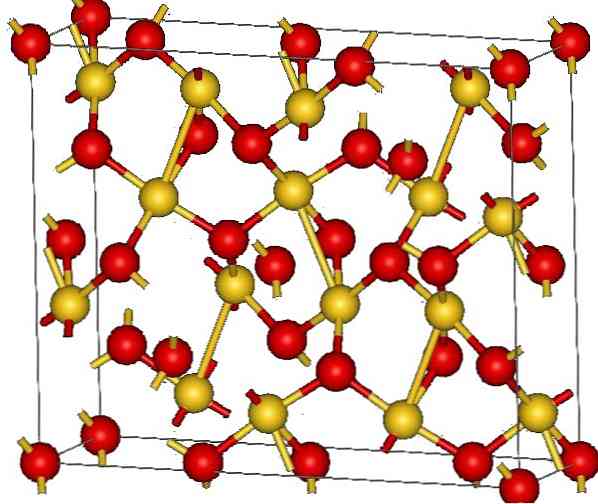
Kristallstrukturen av guld (III) oxid visas i den övre bilden. Arrangemanget av guld- och syreatomerna i det fasta materialet visas antingen som neutrala atomer (kovalent fast substans) eller som joner (joniskt fast ämne). Indistinkt är det tillräckligt att eliminera eller placera Au-O-länkarna i vilket fall som helst.
Enligt bilden antas det att den kovalenta karaktären dominerar (vilket skulle vara logiskt). Av den anledningen är de representerade atomen och bindningarna visade med sfärer respektive staplar. De gyllene sfärerna motsvarar guldatomerna (AuIII-O), och rödaktig till syreatomer.
Om du tittar noggrant ser du att det finns AuO-enheter4, vilka förenas med syreatomer. Ett annat sätt att visualisera det skulle vara att överväga att varje Au3+ är omgiven av fyra O2-; Naturligtvis, från ett joniskt perspektiv.
Denna struktur är kristallin eftersom atomerna är beordrade att lyda samma långdistansmönster. Sålunda motsvarar dess enhetscell det rhomboedrale kristallina systemet (samma som i den övre bilden). Därför är alla Au2O3 kan byggas om alla sfärer av enhetscellen fördelades i rymden.
Elektroniska aspekter
Guld är en övergångsmetall, och det kan förväntas att dess 5d-orbitaler interagerar direkt med syreatomens 2p-orbitaler. Denna överlappning av sina orbitaler borde teoretiskt generera ledningsband som skulle konvertera Au2O3 i en fast halvledare.
Därför är den äkta strukturen hos Au2O3 är ännu mer komplex med detta i åtanke.
hydrater
Guldoxid kan behålla vattenmolekyler i sina romboedrale kristaller, vilket ger upphov till hydrater. När sådana hydrater bildas blir strukturen amorf, det vill säga oordnad.
Kemisk formel för sådana hydrater kan vara något av följande, som i själva verket inte klart förtydligas: Au2O3∙ zH2O (z = 1, 2, 3, etc.), Au (OH)3, eller AuxOoch(OH)z.
Formeln Au (OH)3 representerar en förenkling av den sanna sammansättningen av hydraten. Detta beror på att inom ramen för guldhydroxiden (III) har forskare också funnit närvaron av Au2O3; och därför är det vettigt att behandla det isolerat som en "enkel" övergångsmetallhydroxid.
Å andra sidan av ett fast ämne med formel AuxOoch(OH)z en amorf struktur kunde förväntas eftersom detta beror på koefficienterna x, och och z, vars variationer skulle ge upphov till alla slags strukturer som knappast kunde uppvisa ett kristallint mönster.
egenskaper
Fysiskt utseende
Det är en rödbrun fast substans.
Molekylmassa
441,93 g / mol.
densitet
11,34 g / ml.
Smältpunkt
Det smälter och sönderdelas vid 160ºC. Det saknar därför kokpunkt, så denna oxid når aldrig kokpunkten.
stabilitet
Au2O3 det är termodynamiskt instabil, eftersom guldet, som nämnts i början, inte tenderar att oxidera under normala temperaturförhållanden. Så det är lätt reducerat för att bli igen det ädla guldet.
Ju högre temperaturen desto snabbare reaktionen, som är känd som termisk sönderdelning. Så, Au2O3 vid 160 ° C sönderdelas det för att framställa metalliskt guld och släppa molekylärt syre:
2 Au2O3 => 4 Au + 3 O2
En mycket liknande reaktion kan uppstå med andra föreningar som gynnar nämnda reduktion. Varför reduktion? Eftersom guldet återvänder för att få elektronerna som syre tog bort från det; vilket är detsamma som att det förlorar kopplingar till syre.
löslighet
Det är en fast olöslig i vatten. Det är emellertid lösligt i saltsyra och salpetersyra, på grund av bildandet av guldklorider och nitrater.
nomenklatur
Guldoxid (III) är namnet som regleras av lagernomenklaturen. Andra sätt att nämna det är:
-Traditionell nomenklatur: aureroxid, eftersom valensen 3+ är den högsta för guld.
-Systematisk nomenklatur: diotrioxid.
tillämpningar
Färgläggning av glasögon
En av dess mest framträdande användningsområden är att ge röda färger till vissa material, till exempel glasögon, förutom att ge vissa egenskaper som är inneboende för guldatomerna..
Syntes av aurates och fulminating guld
Om Au läggs till2O3 till ett medium där det är lösligt, och i närvaro av metaller kan urvalerna utfällas efter tillsats av en stark bas; vilka bildas av AuO-anjoner4- i form av metalliska katjoner.
Även Au2O3 reagerar med ammoniak för att bilda den guld-fulminerande föreningen, Au2O3(NH3)4. Dess namn härrör från det faktum att det är mycket explosivt.
Hantering av självmonterade monolager
På guld och dess oxid adsorberas vissa föreningar, såsom dialkyldisulfider, RSSR, inte på samma sätt. När denna adsorption uppträder bildas en Au-S-bindning spontant, där svavelatomen uppvisar och definierar de kemiska egenskaperna hos ytan beroende på den funktionella gruppen till vilken den är bunden..
RSSR kan inte adsorbera på Au2O3, men på metalliskt guld. Om ytan av guldet och dess oxidationsgrad är modifierad, så är storleken hos partiklarna eller skikten av Au2O3, en mer heterogen yta kan utformas.
Denna yta Au2O3-AuSR samverkar med metalloxiderna av vissa elektroniska enheter och utvecklar sålunda framtida smartare ytor.
referenser
- Wikipedia. (2018). Guld (III) oxid. Hämtad från: en.wikipedia.org
- Kemisk formulering (2018). Guldoxid (III). Återställd från: formulacionquimica.com
- D. Michaud. (24 oktober 2016). Guldoxider. 911 Metallurgist. Hämtad från: 911metallurgist.com
- Shi, R. Asahi och C. Stampfl. (2007). Egenskaper hos guldoxiderna Au2O3 och Au2O: Första principen undersökning. Det amerikanska fysiska samhället.
- Cook, Kevin M. (2013). Guldoxid som ett maskeringslager för regioselektiv ytkemi. Avhandlingar och avhandlingar. Papper 1460.


