Silveroxid (Ag2O) struktur, egenskaper, nomenklatur och användningsområden
den silveroxid är en oorganisk förening vars kemiska formel är Ag2O. Kraften som förenar sina atomer är av en helt jonisk natur; Därför består den av ett joniskt fast material där det finns ett förhållande mellan två Ag-katjoner+ interagerar elektrostatiskt med en anjon O2-.
Oxidanjonen, O2-, det härrör från samspelet mellan ytornas silveratomer och omgivningen av syre; på ett mycket liknande sätt som järn och många andra metaller. Ett silverstycke eller smycken istället för att rodna och smula i rost, blir svart, som är karakteristisk för silveroxid.

Till exempel, i bilden ovan kan du se en rostig silver kopp. Notera sin svarta yta, även om den fortfarande behåller något prydnadsglas vilket är anledningen till att även rostiga silverobjekt kan betraktas som attraktiva nog för dekorativa användningsområden.
Egenskaperna av silveroxid är sådana att de inte förstör vid första ögonkastet den ursprungliga metalliska ytan. Den bildas vid rumstemperatur genom enkel kontakt med syret i luften; och ännu mer intressant kan den sönderfalla vid höga temperaturer (över 200 ° C).
Detta innebär att om glaset på bilden hölls och värmen från en intensiv flamma applicerades, skulle den återhämta sin silvery glans. Därför är dess bildning en termodynamiskt reversibel process.
Silveroxid har också andra egenskaper och förutom sin enkla Ag-formel2Eller det omfattar komplexa strukturella organisationer och en stor mängd fasta ämnen. Men Ag2Eller är det kanske, bredvid Ag2O3, den mest representativa för silveroxiderna.
index
- 1 Struktur av silveroxid
- 1.1 Förändringar med antalet valencia
- 2 Fysikaliska och kemiska egenskaper
- 2,1 Molekylvikt
- 2.2 Utseende
- 2,3 Täthet
- 2.4 Smältpunkt
- 2,5 kps
- 2.6 Löslighet
- 2,7 kovalent karaktär
- 2,8 nedbrytning
- 3 nomenklaturen
- 3.1 Valencias I och III
- 3.2 Systematisk nomenklatur för komplexa silveroxider
- 4 användningsområden
- 5 referenser
Struktur av silveroxid
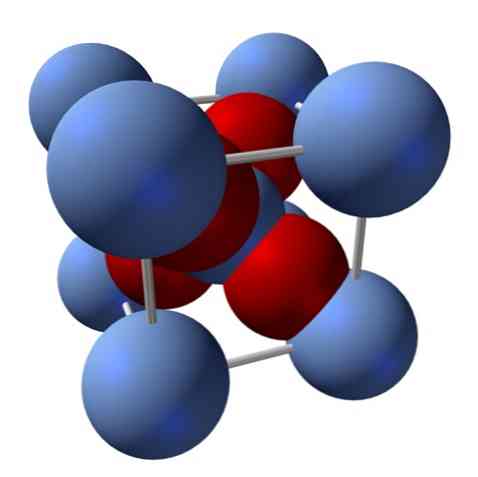
Hur är dess struktur? Som nämnts i början: det är en jonisk fast substans. Av detta skäl kan det inte finnas kovalenta bindningar Ag-O eller Ag = O i sin struktur; eftersom, om det fanns, egenskaperna hos denna oxid skulle förändras drastiskt. Det är då Agioner+ och O2- i ett förhållande 2: 1 och upplever en elektrostatisk attraktion.
Strukturen av silveroxiden bestäms som en följd av det sätt på vilket de joniska krafterna slänger ut i utrymmet Ag-jonerna+ och O2-.
I den övre bilden har du till exempel en enhetscell för ett kubiskt kristallint system: Ag kationerna+ är de silverblå sfärerna och O2- de rödaktiga sfärerna.
Om du räknar antalet sfärer hittar du att det vid första anblicken finns nio silverfärgade och fyra röda färger. Emellertid beaktas endast fragmenten av de sfärer som finns i kuben; att räkna dessa, som är fraktioner av de totala sfärerna, måste förhållandet 2: 1 för Ag uppnås2O.
Upprepa den strukturella enheten av AgO tetraederen4 omgiven av fyra andra Ag+, allt svart solid är byggt (för att undanröja de luckor eller oegentligheter som dessa kristallarrangemang kan ha).
Förändringar med antalet valencia
Fokuserar nu inte på AgO tetraederen4 men i AgOAg linje (se toppunkterna hos den övre navet), kommer att ha den fasta silveroxid består, från ett annat perspektiv, flerskikts jon linjärt anordnade (även benägna). Allt detta som en följd av "molekylär" geometri runt Ag+.
Ovanstående har bekräftats av flera studier av dess jonstruktur.
Silver fungerar övervägande med valens +1, eftersom när man förlorar en elektron är den resulterande elektroniska konfigurationen [Kr] 4d10, vilket är mycket stabilt. Andra valenser, som Ag2+ och Ag3+ de är mindre stabila eftersom de förlorar elektroner från orbitaler nästan helt fyllda.
Agionen3+, Det är emellertid relativt mindre instabil jämfört med Ag2+. Faktum är att det kan samexistera i Ags sällskap+ Kemiskt berikande strukturen.
Den elektroniska konfigurationen är [Kr] 4d8, med oparmade elektroner på ett sådant sätt att det ger en viss stabilitet.
Till skillnad från linjära geometrier runt Agioner+, det har blivit konstaterat att agionerna3+ Det är kvadratiskt platt. Därför en silveroxid med Agjoner3+ skulle bestå av lager bestående av AgO kvadrater4 (ej tetrahedra) elektrostatiskt kopplad av AgOAg-linjer; Sådan är fallet med Ag4O4 eller Ag2O ∙ Ag2O3 med monoklinisk struktur.
Fysikaliska och kemiska egenskaper

Om ytan av silverkoppen skrapade huvudbilden, ett fast ämne, som inte bara är svart, men också har bruna eller bruna (överst) nyanser erhålls. Några av dess fysikaliska och kemiska egenskaper som rapporteras av stunderna är följande:
Molekylvikt
231 735 g / mol
utseende
Solid svart brun i pulverform (observera att trots att det är ett joniskt fast material saknar det ett kristallint utseende). Det är luktfritt och blandat med vatten ger det en metallisk smak
densitet
7,14 g / ml.
Smältpunkt
277-300 ° C Visst smälter det i fast silver; det vill säga bryts det förmodligen innan man bildar flytande oxid.
kps
1,52 ∙ 10-8 i vatten vid 20 ° C Det är därför en förening som är knappt löslig i vatten.
löslighet
Om du ser noggrant på bilden av dess struktur kommer du att finna att sfärerna av Ag2+ och O2- De är inte oense nästan i storlek. Som ett resultat kan endast små molekyler penetrera det inre av det kristallina gitteret, vilket gör det olösligt i nästan alla lösningsmedel; förutom de där det reagerar, såsom baser och syror.
Kovalent karaktär
Fastän det flera gånger har sagts att silveroxid är en jonförening, motsäger vissa egenskaper, såsom dess låga smältpunkt, detta uttalande.
Visserligen överväger övervägande av den kovalenta karaktären inte vad som förklaras för dess struktur, det skulle vara tillräckligt att lägga till strukturen hos Ag2Eller en modell av sfärer och staplar för att indikera kovalenta bindningar.
Även tetraeder- och kvadratplanen AgO4, såväl som AgOAg-linjerna, skulle de vara kopplade med kovalenta (eller kovalenta joniska) bindningar.
Med detta i åtanke, Ag2Eller det skulle faktiskt vara en polymer. Det är emellertid rekommenderat att betrakta det som en jonisk fast substans med kovalent karaktär (vars karaktär av länken är fortfarande en utmaning numera).
sönderdelning
Först nämndes att dess bildning är termodynamiskt reversibel, så det absorberar värme för att återgå till dess metalliska tillstånd. Allt detta kan uttryckas av två kemiska ekvationer för sådana reaktioner:
4Ag (s) + O2(g) => 2Ag2O (s) + Q
2AG2O (s) + Q => 4Ag (s) + O2(G)
Där Q representerar värmen i ekvationen. Detta förklarar varför elden som bränner ytan av den rostade silverkoppen ger sin silverglans tillbaka.
Därför är det svårt att anta att det finns Ag2O (l) eftersom det skulle sönderfalla omedelbart genom värme; om inte trycket är för högt för erhållande av den svarta svarta vätskan.
nomenklatur
När möjligheten till agioner infördes2+ och Ag3+ förutom den gemensamma och dominerande ag+, Begreppet "silveroxid" börjar inte vara tillräckligt för att referera till Ag2O.
Detta beror på att agionen+ är rikligare än de andra, så Ag är taget2Eller som den enda oxiden; vilket inte är korrekt alls.
Om du anser ag2+ som praktiskt taget obefintlig med tanke på dess instabilitet, kommer endast jonerna med valens +1 och +3 att vara närvarande; det vill säga Ag (I) och Ag (III).
Valencias I och III
Att vara Ag (I) minsta valens heter den genom att lägga till suffixet -os till sitt namn Argentum. Så, Ag2Eller det är: argentosooxid eller, enligt den systematiska nomenklaturen, diplatmonoxid.
Om Ag (III) helt ignoreras måste dess traditionella nomenklatur vara: silveroxid istället för argentinoxid.
Å andra sidan är Ag (III) den större valensen adderad suffix -ico till dess namn. Så, Ag2O3 är: silveroxid (2 Agjoner)3+ med tre o2-). Dessutom skulle dess namn enligt den systematiska nomenklaturen vara: diplatatrioxid.
Om strukturen hos Ag observeras2O3, det kan antas att det är oxidationsprodukten av ozon, OR3, istället för syre. Därför måste dess kovalenta karaktär vara större eftersom det är en kovalent förening med Ag-O-O-O-Ag eller Ag-O-bindningar.3-Ag.
Systematisk nomenklatur för komplexa silveroxider
AgO, också skrivet som Ag4O4 eller Ag2O ∙ Ag2O3, Det är en silveroxid (I, III), eftersom den har både valens +1 och +3. Dess namn enligt den systematiska nomenklaturen skulle vara: tetraplattetraoxid.
Denna nomenklatur är till stor hjälp när det gäller andra stökiometriskt mer komplexa silveroxider. Antag exempelvis de två fastämnena 2Ag2O ∙ Ag2O3 och Ag2O ∙ 3Ag2O3.
Att skriva den första på ett mer lämpligt sätt skulle vara: Ag6O5 (räknar och adderar atomer av Ag och O). Hans namn skulle då vara hexaplatpentoxid. Observera att denna oxid har en silverkomposition mindre rik än Ag2O (6: 5 < 2:1).
Medan du skriver den andra fasten annars skulle det vara: Ag8O10. Dess namn skulle vara oktaplatdekaoxid (med ett förhållande 8:10 eller 4: 5). Denna hypotetiska silveroxid skulle vara "mycket oxiderad".
tillämpningar
Studier på jakt efter nya och sofistikerade användningsområden för silveroxid utförs fortfarande idag. Några av dess användningsområden är listade nedan:
-Det löses i ammoniak, ammoniumnitrat och vatten för att bilda Tollens-reagenset. Detta reagens är ett användbart verktyg vid kvalitativa analyser inom organiska kemi laboratorier. Det tillåter att bestämma närvaron av aldehyder i ett prov, varvid det positiva svaret är bildandet av en "silverspegel" i provröret.
-Tillsammans med metallisk zink bildar den de primära batterierna av zinkoxid av silver. Detta är kanske en av de vanligaste och hemma användningarna.
-Det tjänar som en gasrenare, som absorberar till exempel CO2. Vid uppvärmning frigörs de fångade gaserna och kan återanvändas flera gånger.
-På grund av de antimikrobiella egenskaperna hos silver är dess oxid användbar i studier av bioanalys och markrening.
-Det är ett milt oxidationsmedel som kan oxidera aldehyder till karboxylsyror. Det används också i Hofmann-reaktionen (tertiära aminer) och deltar i andra organiska reaktioner, antingen som reagens eller katalysator.
referenser
- Bergstresser M. (2018). Silveroxid: Formel, sönderdelning och formation. Study. Hämtad från: study.com
- Författare och redaktörer av volymerna III / 17E-17F-41C. (N.D.). Silveroxider (Ag (x) O (y)) kristallstruktur, gitterparametrar. (Numeriska data och funktionella relationer i vetenskap och teknik), vol 41C. Springer, Berlin, Heidelberg.
- Mahendra Kumar Trivedi, Rama Mohan Tallapragada, Alice Branton, Dahryn Trivedi, Gopal Nayak, Omprakash Latiyal, Snehasis Jana. (2015). Potentiella effekter av biofältens energibehandling på fysikaliska och termiska egenskaper hos silveroxidpulver. International Journal of Biomedical Science and Engineering. Volym 3, nr 5, sid. 62-68. doi: 10.11648 / j.ijbse.20150305.11
- Sullivan R. (2012). Nedbrytning av silveroxid. University of Oregon Hämtad från: chemdemos.uoregon.edu
- Flint, Deyanda. (24 april 2014). Användningar av silveroxidbatterier. Sciencing. Hämtad från: sciencing.com
- Salman Montasir E. (2016). Studie av några optiska egenskaper hos silveroxid (Ag2o) med användning av UVVisible spektrofotometer. [PDF]. Hämtad från: iosrjournals.org
- Bard Allen J. (1985). Standardpotential i vattenlösning. Marcel Dekker. Hämtad från: books.google.co.ve


