Etyleteregenskaper, struktur, erhållande, användningar
den etyleter, även känd som dietyleter, är en organisk förening vars kemiska formel är C4H10O. Det kännetecknas av att vara en färglös och flyktig vätska, och därför måste dess flaskor hållas stängda så hermetiskt som möjligt.
Denna eter klassificeras som en medlem av dialkyletrarna; det vill säga de har formeln ROR ', där R och R' representerar olika kolsegment. Och som det beskriver sitt mellannamn, dietyleter, är två radikaler-etyl de som binder till syreatomen.

Ursprungligen användes etyleter som en allmän bedövning, introducerad 1846 av William Thomas Green Morton. På grund av dess brandfarlighet avvisades dess användning, men ersatte den med andra mindre farliga bedövningsmedel..
Denna förening har också använts för att uppskatta tiden för blodcirkulationen, under bedömningen av patienternas kardiovaskulära status.
Inuti kroppen kan dietyleter omvandlas till koldioxid och metaboliter; den senare hamnar utsöndras i urinen. Emellertid är det mesta av den eter som administreras utandas i lungorna, utan att genomgå någon modifiering.
Å andra sidan användes det som lösningsmedel för tvål, oljor, parfymer, alkaloider och gummin.
index
- 1 Struktur av etyleter
- 1.1 Intermolekylära krafter
- 2 Fysikaliska och kemiska egenskaper
- 2.1 Andra namn
- 2,2 Molekylformel
- 2,3 Molekylvikt
- 2.4 Fysisk utseende
- 2,5 lukt
- 2.6 Smak
- 2,7 kokpunkt
- 2,8 smältpunkt
- 2.9 Flampunkt
- 2.10 Löslighet i vatten
- 2.11 Löslighet i andra vätskor
- 2,12 Densitet
- 2.13 Ångdensitet
- 2.14 Ångtryck
- 2,15 Stabilitet
- 2.16 Automatisk tändning
- 2.17 Nedbrytning
- 2,18 Viskositet
- 2.19 Förbränningsvärme
- 2.20 Förångningsvärme
- 2.21 Ytspänning
- 2.22 Joniseringspotential
- 2.23 Luktgräns
- 2.24 brytningsindex
- 3 Erhållande
- 3.1 Från etylalkohol
- 3.2 Från etylen
- 4 Toxicitet
- 5 användningar
- 5,1 organiskt lösningsmedel
- 5.2 Allmän anestesi
- 5.3 Eterens ande
- 5.4 Utvärdering av blodcirkulationen
- 5.5 Undervisningslaboratorier
- 6 referenser
Struktur av etyleter
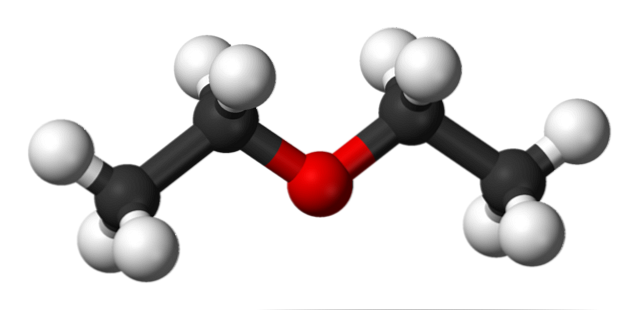
I bilden ovan har vi en representation med en modell av sfärer och stänger av etyleternas molekylstruktur.
Såsom kan ses, har den röda sfären, som motsvarar syreatomen, två etylgrupper kopplade på båda sidor. Alla länkar är enkla, flexibla och fritt roterbara runt axlarna σ.
Dessa rotationer härstammar stereoisomerer kända som konformatorer; att mer än isomerer, de är alternativa rumsliga stater. Bildens struktur motsvarar exakt den anti-konformare, där alla dess atomergrupper är förskjutna (separerade från varandra).
Vad skulle vara den andra konformaren? Eclipsed, och även om din bild inte är tillgänglig, visualiserar du den med U-form. Vid de övre ändarna av U skulle du hitta metylgrupperna, -CH3, som skulle uppleva steriska repulsioner (de skulle kollidera i rymden).
Därför förväntas att CH-molekylen3CH2OCH2CH3 anta anti konformationen större delen av tiden.
Intermolekylära krafter
Med vilka intermolekylära styrkor regleras molekylerna av etyleter i vätskefasen? De bibehålls i vätskan huvudsakligen tack vare dispersionskrafterna, eftersom deras dipolmoment (1,5D) saknar en region som är tillräckligt bristfällig i elektronisk densitet (8 +)
Detta beror på att ingen kolatom i etylgrupperna ger för mycket elektrondensitet till syreatomen. Ovanstående är uppenbart med kartan över elektrostatisk potential av etyleter till hands (bottenbild). Observera frånvaron av en blå region.
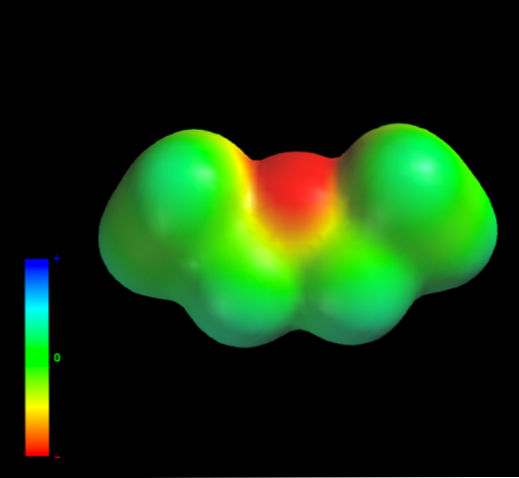
Syre kan inte heller bilda vätebindningar, eftersom det inte finns några tillgängliga O-H-bindningar i molekylstrukturen. Därför är det de momentana dipolerna och deras molekylmassa som gynnar deras spridningskrafter.
Trots detta är det mycket lösligt i vatten. Varför? Eftersom dess syreatom, med en högre elektrondensitet, kan acceptera vätebindningar från en vattenmolekyl:
(CH3CH2)2Oδ- - δ+H-OH
Dessa interaktioner ansvarar för 6,04 g av denna eter som löses i 100 ml vatten.
Fysikaliska och kemiska egenskaper
Övriga namn
-Dietyleter
-etoxietan
-Etyloxid
Molekylformel
C4H10O eller (C2H5)2O.
Molekylvikt
74,14 g / mol.
Fysiskt utseende
Färglös vätska.
lukt
Söt och kryddig.
smak
Brännande och söt.
Kokpunkt
94,3 ºF (34,6 ºC) till 760 mmHg.
Smältpunkt
-177,3 ºF (-116,3 ªC). Stabila kristaller.
Tändpunkt
-49ºF (sluten behållare).
Löslighet i vatten
6,04 g / 100 ml vid 25 ° C.
Löslighet i andra vätskor
Blandbar med kortkedjiga alifatiska alkoholer, bensen, kloroform, petroleumeter, fettlösningsmedel, många oljor och koncentrerad saltsyra.
Lösligt i aceton och mycket lösligt i etanol. Det är också lösligt i nafta, bensen och oljor.
densitet
0,714 mg / ml vid 68 ªF (20 ºC).
Ångdensitet
2,55 (i förhållande till luft tagen med densitet 1).
Ångtryck
442 mmHg vid 68ºF. 538 mmHg vid 25 ° C. 58,6 kPa vid 20 ºC.
stabilitet
Det oxideras långsamt genom luft, fukt och ljus med bildandet av peroxider.
Bildningen av peroxider kan förekomma i eterbehållare som har öppnats och förvaras i mer än sex månader. Peroxider kan detonera genom friktion, slag eller uppvärmning.
Undvik kontakt med: zink, halogener, icke-metalliska oxihalhalider, starka oxidationsmedel, kromylklorid, tementinoljor, nitrater och metallklorider.
Automatisk tändning
356ºF (180ºC).
sönderdelning
Vid uppvärmning sönderdelas det, vilket ger en skarp och irriterande rök.
viskositet
0,2444 cPoise vid 20 ºC.
Förbränningsvärme
8 807 Kcal / g.
Förångningsvärme
89,8 cal / g vid 30 ºC.
Ytspänning
17,06 dyn / cm vid 20 ° C.
Joniseringspotential
9,53 eV.
Lukttröskel
0,83 ppm (renhet ges ej).
Brytningsindex
1,355 vid 15 ºC.
erhålla
Från etylalkohol
Etyleter kan erhållas från etylalkohol, i närvaro av svavelsyra som en katalysator. Svavelsyran i ett vattenhaltigt medium dissocierar att producera hydroniumjonen, H3O+.
Den vattenfria etylalkoholen strömmar genom svavelsyralösningen, upphettad mellan 130 ° C och 140 ° C, vilket ger protonering av etylalkoholmolekyler. Därefter reagerar en annan molekyl av icke-protonerad etylalkohol med den protonerade molekylen.
När detta händer främjar den nukleofila attacken av den andra molekylen av etylalkohol frisättning av vatten från den första molekylen (den protonerade); som ett resultat bildas en protonerad etyleter (CH3CH2OHCH2CH3), med partiellt laddad syrepositiv.
Emellertid förlorar denna syntesmetod effektivitet eftersom svavelsyran utspädes med det vatten som produceras under processen (produkt av dehydrering av etylalkohol).
Reaktionstemperaturen är kritisk. Vid temperaturer under 130 ° C är reaktionen långsam och i huvudsak destilleras etylalkohol.
Över 150 ° C orsakar svavelsyra bildningen av etylen (dubbelbindningen alken) i stället för att kombinera med etylalkohol för att bilda etyleter.
Från eten
I motsats till det vill säga kan hydrering av eten i ångfasen, etyleter bildas som en biprodukt förutom etylalkohol. I själva verket producerar denna syntetiska väg det mesta av denna organiska förening.
Denna process använder fosforsyrakatalysatorer fixerade till en fast bärare, som kan justeras för att producera mer eter.
Dehydrering i ångfas av etanol i närvaro av aluminiumoxidkatalysatorer kan ge ett utbyte på 95% vid framställning av etyleter.
toxicitet
Det kan ge irritation på huden och ögonen genom kontakt. Kontakt med huden kan orsaka torkning och sprickbildning. Etern tränger vanligtvis inte in i huden, eftersom det snabbt indunstas.
Irriteringen av ögonen orsakad av etern är vanligtvis mild, och i händelse av allvarlig irritation är skadan oftast reversibel.
Dess intag ger narkotiska effekter och mag irritation. Allvarlig förtäring kan orsaka njurskador.
Inandning av eter kan orsaka irritation i näsa och hals. Vid inandning av eter kan uppstå: sömnighet, spänning, yrsel, kräkningar, oregelbunden andning och ökad salivation.
Hög exponering kan orsaka förlust av medvetande och till och med död.
OSHA fastställer en exponeringsgräns på 800 ppm i genomsnitt under en 8 timmars skift.
Nivåer av ögonirritation: 100 ppm (human). Nivån av ögonirritation: 1200 mg / m3 (400 ppm).
tillämpningar
Organiskt lösningsmedel
Det är ett organiskt lösningsmedel som används för att lösa upp brom, jod och andra halogener. Majoriteten av lipider (fetter), hartser, rena gummin, vissa alkaloider, gummin, parfymer, cellulosaacetat, cellulosa nitrat, kolväten och färgämnen.
Dessutom används den vid utvinning av de aktiva principerna för animaliska vävnader och växter, eftersom den har en lägre densitet än vatten och flyter på den, vilket lämnar de önskade substanserna upplösta i etern.
Allmänna anestesi
Den har använts som allmänbedövning sedan 1840, ersatt kloroform för att ha en terapeutisk fördel. Det är emellertid ett brandfarligt ämne och upplever därför allvarliga svårigheter för användning inom kliniska miljöer.
Dessutom producerar det hos patienter några oönskade postoperativa biverkningar som illamående och kräkningar.
Av dessa skäl har användningen av eter som allmänbedövning kasseras, ersatt den med andra bedövningsmedel, såsom halotan..
Eterens ande
Eter blandad med etanol användes för att bilda lösningen kallad eter av eter, som användes vid behandling av gastrisk flatulens och mildare former av gastralgi.
Utvärdering av blodcirkulationen
Eter har använts för att utvärdera blodcirkulationen mellan en arm och lungorna. Eteren injiceras i en arm och leder blodet till höger atrium, sedan till höger kammare och därifrån till lungorna.
Den tid som går från injektionen av etern till upptaget av eterluften i utandad luft är ungefär 4 till 6 s.
Undervisningslaboratorier
Eter används i undervisningslaboratorier i många experiment; till exempel vid demonstration av Mendels genetiska lagar.
Eteren används för att numera flugorna i släktet Drosophila och tillåta nödvändiga korsningar mellan dem, för att bevisa genetiska lagar
referenser
- Graham Solomons T.W., Craig B. Fryhle. (2011). Organisk kemi. Aminer. (10th upplagan.). Wiley Plus.
- Carey F. (2008). Organisk kemi (Sjätte upplagan). Mc Graw Hill.
- The Sevier. (2018). Dietyleter. Science Direct. Hämtad från: sciencedirect.com
- Editors of Encyclopaedia Britannica. (2018). Etyleter. Britannica ncyclopædia. Hämtad från: britannica.com
- PubChem (2018). Eter. Hämtad från: pubchem.ncbi.nlm.nih.gov
- Wikipedia. (2018). Dietyleter. Hämtad från: en.wikipedia.org
- Säkerhetsblad XI: etyleter. [PDF]. Återställd från: quimica.unam.mx


