Ziehl-Neelsen Stain Foundation, reagenser och teknik
den Ziehl-Neelsen fläck i en färgteknik för att identifiera alkoholbaserade resistenta mikroorganismer (AAR). Namnet på denna mikrobiologiprocess hänvisar till dess författare: bakteriologen Franz Ziehl och patologen Friedrich Neelsen.
Denna teknik är ett slags differential färgning, vilket innebär användning av olika färger för att skapa kontrast mellan strukturer som vill observera, identifiera och därefter differentiera. Ziehl-Neelsen fläck används för att identifiera vissa typer av mikroorganismer.
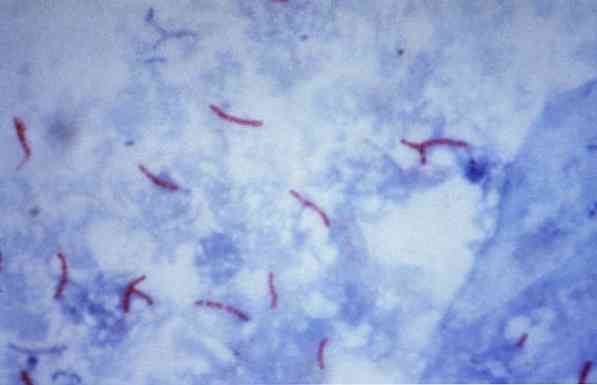
Några av dessa mikroorganismer är mykobakterier (till exempel, Mycobacterium tuberculosis), nocardier (till exempel, Nocardia sp.) och några unicellulära parasiter (till exempel, Cryptosporidium parvum). Många av bakterierna kan klassificeras genom en vanlig teknik som kallas Gram stain.
Men vissa bakteriegrupper kräver andra metoder för att identifiera dem. Tekniker som Ziehl-Neelsen-färgning kräver kombinationer av färgämnen med värme för att fixa den första till cellväggen.
Sedan kommer en missfärgningsprocess som ger två resultat: motstånd eller känslighet för missfärgning av syror och alkoholer.
index
- 1 Stiftelsen
- 1.1 Sekundär färgning
- 2 reagenser
- 2.1 Primär färgning
- 2.2 Avfärgningslösning
- 2.3 Sekundär färgning (anti-färgämne)
- 3 Teknik
- 3.1 Acid-snabb färgningsprocedur
- 4 referenser
foundation
Grunden för denna färgningsteknik är baserad på dessa väggers egenskaper hos dessa mikroorganismer. Väggen bildas av en typ av fettsyror som kallas mykola syror; Dessa kännetecknas av mycket långa kedjor.
När fettsyror har mycket långa strukturer, kan de bibehålla färgämnen lättare. Någon genera av bakterier är mycket svår att fläcka genom Gram-fläck, på grund av den höga mykolsyrahalten i cellväggen.
I Ziehl-Neelsen-fläcken används fenolföreningen carbol fuchsin, en basfärg. Detta har förmågan att interagera med cellens väggfettsyror, vilket är vaxartad struktur vid rumstemperatur.
Karbolfuksin färgning förbättras i närvaro av värme, eftersom vaxet smälter och färgämnesmolekylerna röra sig snabbare i cellväggen.
Syran som används senare tjänar till att missfärga cellerna som inte färgades eftersom deras vägg inte var tillräckligt relaterad till färgämnet; Därför är styrkan hos syraavfärgningsmedlet i stånd att avlägsna syrafärgämnet. De celler som motstår denna missfärgning kallas syrafast.
Sekundär färgning
Efter missfärgning av provet står detta i kontrast med ett annat färgämne som kallas sekundärt färgämne. Methylenblå eller malakitgrön används vanligtvis.
Det sekundära färgämnet fläckar bakgrundsmaterialet och skapar följaktligen kontrast till de strukturer som färgades i det första steget. Endast de missfärgade cellerna absorberar det andra färgämnet (anti-fläck) och tar sin färg, medan de syrafasta cellerna behåller den röda färgen.
Denna procedur används ofta för identifiering av Mycobacterium tuberculosis och Mycobacterium leprae, som kallas syrafasta baciller.
reagens
Primär färgning
Karboxin 0,3% fuchsin (filtrerad) användes. Detta färgämne framställdes från en blandning av alkoholer: fenol i etanol (90%) eller metanol (95%), och denna blandning löstes 3 g basiskt fuksin.
Avfärgningslösning
I detta steg kan du använda lösningar av 3% alkoholsyra eller 25% svavelsyra.
Sekundär färgning (anti-färgämne)
Färgen som vanligtvis används för att utföra kontrast i proverna är vanligtvis 0,3% metylenblå. Men andra kan också användas, såsom 0,5% malakitgrön.
teknik
Acid-snabb färgningsprocedur
Förbered en bakteriell smet
Denna beredning görs på en ren och torr glidning, efter sterilitetsföreskrifter.
Torka smeten
Låt smeten torka vid rumstemperatur.
Värm provet
Provet måste värmas genom att man sätter eld på bilden nedan. Det kan göra en fixering med alkohol när smear inte har upprättats med slem (behandlad med natriumhypoklorit för att bleka) och om inte omedelbart vara färgad.
M. tuberculosis Det elimineras med blekmedel och under färgprocessen. Termofixering av obehandlat sputum kommer inte att döda M. tuberculosis, medan fixering med alkohol är bakteriedödande.
Täck fläcken
Fläcken är täckt med carbol fuchsinlösningen (primär grundläggande fläck).
Värm fläcken
Detta görs i 5 minuter. Du bör märka en ångavgivning (ca 60 ° C). Det är viktigt att inte överhettas och undviker att bränna provet.
Om uppvärmningen av fläcken måste vara mycket noga med att värma karbolfuksin, speciellt om färgningen utföres på en bricka eller annan behållare i vilken den samlades mycket brandfarliga kemikalier föregående infärgning.
Endast en liten flamma bör appliceras under glidbanorna med hjälp av en tänd swab som tidigare fuktats med några droppar syraalkohol, metanol eller 70% etanol. Undvik att använda en stor vattentank som är nedsänkt i etanol eftersom detta är en brandrisk.
Tvätta fläcken
Denna tvättning bör ske med rent vatten. Om kranvattnet inte är rent, tvätta smetet med filtrerat eller destillerat vatten, helst.
Täck smeten med sur alkohol
Denna syraalkohol bör vara 3%. Täckningen utförs i 5 minuter eller tills smetet är tillräckligt missfärgat, det vill säga blekrosa.
Det måste beaktas att syraalkohol är brandfarlig. Därför måste den användas mycket noggrant. Undvik att vara nära antändningskällor.
Tvätta fläcken
Tvättningen bör vara med rent, destillerat vatten.
Täck smet med färgämne
Det kan vara färgämne i grön malakit (0,5%) eller metylenblå (0,3%) i 1 eller 2 minuter, med den längsta tiden om smeten är tunn.
Tvätta fläcken
Rent vatten måste användas igen (destillerat).
dränera
Torka ut på baksidan av sliden och placera lappen på en hylla avlopp så att denna lufttorka (använd inte absorberande papper för torkning).
Undersök smet i mikroskopet
100X-objektet och nedsänkningsoljan ska användas. Skanna smetet systematiskt och skriv ned relevanta observationer.
Tolka resultaten
Teoretiskt anses mikroorganismer som färgas en rödaktig färg betraktad som syrafast positiv (AAR +).
Tvärtom, om mikroorganismerna är färgade blå eller gröna, beroende på färgämnet som används som ett färgämne, anses de vara negativa alkoholresistenta syror (AAR-).
referenser
- Apurba, S. & Sandhya, B. (2016). Essentials of Practical Microbiology (1: e upplagan). Jaypee Brothers Medical Publishers.
- Bauman, R. (2014). Mikrobiologi med sjukdomar genom kroppssystem (4: e upplagan). Pearson Education, Inc.
- Heritage, J., Evans, E. & Killington, A. (1996). Introduktionell mikrobiologi (1: e upplagan). Cambridge University Press.
- Morello, J., Granato, P. Wilson, M. & Morton, V. (2006). Laboratoriehandbok och arbetsbok i mikrobiologi: ansökningar till patientvård (11: e upplagan). McGraw-Hill Education.
- Vasanthakumari, R. (2007). Textbok av mikrobiologi (1: e upplagan). B.l. Publikationer PVT.


