Aluminiumsulfat (Al2 (SO4) 3) struktur, användningsområden, typer, toxicitet
den aluminiumsulfat är ett oorganiskt aluminiumsalt med formeln Al2(SO4)3, som vanligen framträder som ett vitt fast ämne med glänsande kristaller. Färgen på föreningen kommer att påverkas av dess koncentration av järn och någon annan förorening. Det finns två huvudtyper av aluminiumsulfat: A och B.
I den nedre bilden visas vita kristaller av hydratiserat aluminiumsulfat. Frånvaron av bruna färgämnen, som indikerar järnjoner i det kristallina gitteret, kan noteras.

Aluminiumsulfat är ett salt som är mycket lösligt i vatten och i naturen är det sällsynt att hitta det i vattenfri form. Det hydratiseras vanligen i form av oktadekahydrataluminiumsulfat [Al2(SO4)3.18H2O] eller hexadekahydrat [Al2(SO4)3.16H2O].
På samma sätt kan det bilda dubbla salter med kalium och med ammonium, föreningar som är kända som alun. Till viss del kan detta bero på vattenets affinitet i hydraten för att behålla andra joner förutom aluminium.
Aluminiumsulfat kan brytas ner genom att vattnet påverkar aluminiumhydroxid och svavelsyra. Den här egenskapen har tillåtit dess användning som surgörare av marken.
Det är också en giftig förening, särskilt genom kontakt med dess pulver. Det har emellertid en oändlighet av användningar och tillämpningar som går från rening av vattnet med hjälp av koagulationsmetoden, som sker genom användningen i flera industrier tills dess användning med terapeutiska syften.
index
- 1 struktur
- 2 Vad är det för (användningar)
- 2.1 Koagulering eller flockning av vatten
- 2.2 Använd som ett mord av bläck och vid utarbetandet av papper
- 2.3 Industriella användningsområden
- 2.4 Läkemedel och terapeutiska användningsområden
- 2.5 Andra användningsområden
- 3 Produktion av aluminiumsulfat
- 4 typer
- 5 Toxicitet
- 6 referenser
struktur
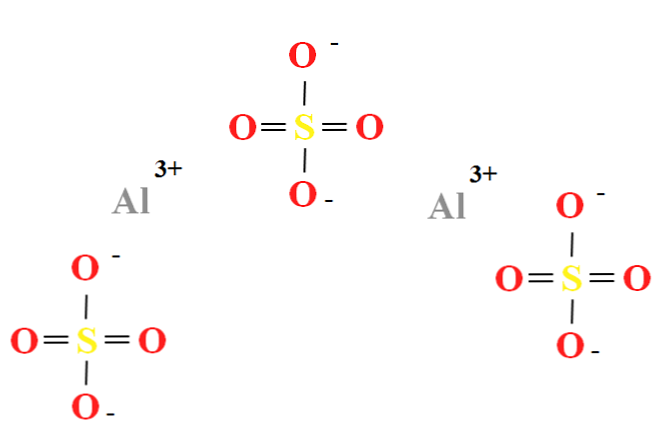
Aluminiumsulfat har ett förhållande av två Al-katjoner3+ för var tredje anjonen SO42- (toppbild), som kan observeras direkt i sin kemiska formel Al2(SO4)3.
Observera att Al3+ de är gråaktiga, medan SO42- de är gula (för svavelatomen) och röda (för syreatomerna).
Den illustrerade strukturen motsvarar den vattenfria formen av Al2(SO4)3, eftersom ingen vattenmolekyl interagerar med joner. I dina hydrater kan dock vattnet lockas till de positiva centra av Al3+, eller av den negativa SO tetrahedra42- genom vätebindningar (HOH-0-SO32-).
Al2(SO4)3∙ 18H2Eller, till exempel, innehåller den 18 vattenmolekyler i sin fasta struktur. Vissa av dem kan vara i direkt kontakt med Al3+ eller med SO42-. Med andra ord: aluminiumsulfat kan ha internt eller externt samordningsvatten.
Dess struktur kan också rymma andra katjoner såsom Fe3+, na+, K+, etc. Men för detta är det nödvändigt närvaron av fler anjoner SO42-. För vad? Att neutralisera ökningen av positiva laddningar på grund av metalliska föroreningar.
Aluminiumsulfat kan ha många strukturer, även om dess hydrater tenderar att anta det monokliniska kristallina systemet.
Fysikaliska och kemiska egenskaper
utseende
Den verkar som en fast substans med ljust vita kristaller, granuler eller pulver.
Molekylvikt
342,31 g / mol (vattenfri).
lukt
Det är luktfritt
smak
Söt smak måttligt astringent.
Smältpunkt
770 ° C vattenfri form (86,5 ° C oktadekahydratform)
Löslighet i vatten
31,2 g / 100 ml vid 0 ° C; 36,4 g / 100 ml vid 20 ° C och 89 g / 100 ml vid 100 ° C.
densitet
2,67 till 2,71 g / cm3.
löslighet
Lite löslig i etylalkohol.
Ångtryck
I huvudsak noll.
stabilitet
Stabil i luften.
sönderdelning
Vid upphettning, vid ungefär dess smältpunkt, kan den sönderdelas genom att emittera särskilt svaveloxid, en giftig gas.
korrosivitet
Aluminiumsulfatlösningar är frätande mot aluminium. Även föreningen kan korrodera metaller i närvaro av fukt.
pKa
3,3 till 3,6. Och dess pH är 2,9 eller mer i en 5% vattenhaltig lösning.
Vad är det för (användningar)
Koagulering eller flockning av vatten
-När blandat med vatten (drickbart, serverat eller avfall) orsakar aluminiumsulfat aluminiumhydroxid, vilket bildar komplex med föreningarna och partiklarna i lösning som accelererar deras sedimentering, vilket i avsaknad av behandling med aluminiumsulfat skulle ta lång tid.
-Aluminiumsulfat används också vid rengöring av poolvatten, vilket gör dem mer attraktiva för användning.
-Genom användning av aluminiumsulfat erhålls vatten utan grumlighet och färg, vilket ökar dess potabilitet genom att underlätta rengöring av vatten. Tyvärr kan denna reningsmetod leda till en något ökad koncentration av aluminium i vattnet.
-Aluminium är en mycket giftig metall som ackumuleras i huden, hjärnan och lungorna och orsakar allvarliga sjukdomar. Dessutom är det inte känt vilken funktion den uppfyller i levande varelser.
-Europeiska unionen kräver att den maximala tillåtna gränsen för aluminium i vatten inte överstiger 0,2 mg / l. Samtidigt kräver US Environmental Protection Agency att den maximala gränsen för vattenföroreningar med aluminium inte överstiger 0,05-0,2 mg / l.
-Behandlingen av avloppsvatten eller användes med aluminiumsulfat möjliggör eliminering eller reduktion av fosfor i dem, ekonomiskt.
Använd som en mordant av bläck och vid utarbetandet av papper
-Aluminiumsulfat har använts som en mordant för färgämnen eller bläck som hjälper till att fixa på det material som ska färgas. Dess fixeringsverkan beror på Al (OH)3, vars gelatinösa konsistens bidrar till adsorption av färgämnen på textilier.
-Även om det har använts sedan omkring 2000 f.kr. för det beskrivna syftet, kräver endast organiska färgämnen mordanter. Syntetiska färgämnen å andra sidan kräver inte mordants att uppfylla sin funktion.
-Den har förskjutits från pappersframställning, men används fortfarande vid produktion av pappersmassa. Avlägsnar föroreningar, liksom har använts för att binda material, neutralisera laddningarna och kalibrera kolofoniumet.
Industriella användningsområden
-Det används i byggbranschen för att påskynda betongens inställning. Dessutom används den i vattentätning av byggnader.
-I tvål och fettindustrin används den vid framställning av glycerin.
-Det används i oljeindustrin vid tillverkning av syntetiska katalysatorer som används under drift.
-Det används i läkemedelsindustrin som en sammandragande vid framställning av droger och kosmetika.
-Intervenerar i framställning av färgämnen som karmin. Det används också som färgämne vid tillverkning av syntetiska gummin av butadienstyren.
-I sockerindustrin används den som en melassrenare för sockerrör.
-Det används vid tillverkning av deodoranter. Varför? Eftersom det orsakar en minskning av svettningskörlarnas kanaler, vilket därigenom begränsar ansamling av svett, ett nödvändigt medium för tillväxt av bakterier som orsakar lukt.
-Den används i läder garvning, den nödvändiga processen för dess användning. Dessutom används den vid tillverkning av gödningsmedel.
-Den används som tillsats vid beredning av färger, lim och tätningsmedel, samt rengörings- och vårdprodukter för möbler..
Läkemedel och terapeutiska användningsområden
-Aluminiumsulfat är ett immunologiskt adjuvans. Därför uppfyller den funktionen att behandla antigenerna på ett sådant sätt att de, när de släpps vid deras verkningsområde, producerar en större produktion av antikroppar för antigenerna som ympades.
-Freunds adjuvans och BCG, liksom andra adjuvanser, inklusive endogena sådana som interleukiner, är icke-specifika för antigener, vilket möjliggör en ökning av immunförsvarets radie. Detta har gjort det möjligt att utveckla vacciner mot många sjukdomar.
-Den koagulerande verkan av aluminiumsulfat har medfört eliminering av många virus i behandlat vatten, bland annat: Q beta, MS2, T4 och P1. Resultaten indikerar att behandling av vatten med aluminiumsulfat ger en inaktivering av sådana virus.
-Aluminiumsulfat används i form av pinne eller som ett pulver vid behandling av små ytliga sår eller slitningar som produceras vid rakning.
-Det används vid tillverkning av aluminiumacetat, en förening som används vid behandling av vissa öronförhållanden. Det har också använts, utan betydande framgång, för att lindra följderna av eldmyrbett..
-Lösningar av aluminiumsulfat används i en koncentration av 5% till 10% vid lokal behandling av sår som tillåter kontroll av deras sekret.
-Den astringenta verkan av aluminiumsulfat kontraherar hudens ytliga skikt, koagulerar proteinerna och läker såren.
Andra användningsområden
-Aluminiumsulfat hjälper till att kontrollera överdriven tillväxt av alger i dammar, sjöar och i vattenflöden. Den används också vid avlägsnande av blötdjur, bland annat den spanska slugan.
-Trädgårdarna tillämpar denna förening för att sura alkaliska jordar. I kontakt med vattnet därav sönderdelas aluminiumsulfatet i aluminiumhydroxid och utspädd svavelsyra. Sedan utfälles aluminiumhydroxiden och lämnar svavelsyran i lösning.
-Försurningen av jordar på grund av svavelsyra visualiseras på ett mycket kreativt sätt, på grund av förekomsten av en växt som kallas Hydrangea, vars blommor blir blåa i närvaro av sur jord; det vill säga de är känsliga och svarar på förändringar i pH.
-Aluminiumsulfat är inblandat i framställning av ett skum för att bekämpa och kontrollera eld. Hur? Reagerar med natriumbikarbonat, vilket ger frisättning av CO2. Denna gas blockerar O-åtkomst2 till förbränningsstället av materialet; och därmed eldupphöret som utvecklades.
Produktion av aluminiumsulfat
Aluminiumsulfat syntetiseras genom att reagera en aluminiumrik förening, såsom bauxitmalm, med svavelsyra vid förhöjda temperaturer. Följande kemiska ekvation representerar reaktionen:
till2O3 + H2SW4 -> Al2(SO4)3 + 3 H2O
Aluminiumsulfat kan även bildas genom en neutraliseringsreaktion mellan aluminiumhydroxid och svavelsyra enligt följande reaktion:
2 Al (OH)3 + 3 H2SW4 + 12 H2O -> Al2(SO4)3.18H2O
Svavelsyra reagerar med aluminium för att bilda ammoniumsulfat och frisättning av vätemolekyler i form av gas. Reaktionen schematiseras enligt följande:
2 Al + 3 H2SW4 -> Al2(SO4)3 + 3 H2
Typ
Aluminiumsulfat klassificeras i två typer: typ A och typ B. I aluminiumsulfat typ A är fastämnena vita och har en järnkoncentration av mindre än 0,5%.
I aluminiumsulfat typ B är fastämnena bruna och har en järnkoncentration av mindre än 1,5%.
Det finns industrier som producerar aluminiumsulfat som har olika kriterier för deras klassificering. Sålunda rapporterar en industri för sin framställning av typ A aluminiumsulfat en maximal koncentration av 0,1% järn som järnoxid. Medan för typ B anger de en maximal järnkoncentration av 0,35%.
toxicitet
-Aluminiumsulfat är en förening som utövar sin giftiga verkan genom kontakt med sitt damm, vilket orsakar hudirritation och i fall där kontakten är frekvent, en dermatit.
-I ögonen orsakar det en stark irritation, även för att orsaka permanenta skador.
-Inandning orsakar irritation i näsan och halsen, vilket kan orsaka hosta och utslag.
-Dess intag orsakar mag irritation, illamående och kräkningar.
-Det finns toxiska effekter som trots att de inte är direkt beroende av aluminiumsulfat, är de indirekt på grund av deras användning. Det här gäller vissa toxiska effekter av aluminium som orsakas av användningen av aluminiumsulfat vid rening av vatten.
-Patienter som kroniskt dialyseras med användning av salter framställda i renat vatten, genom användning av aluminiumsulfat, upplever mycket allvarliga hälsosjukdomar. Bland dessa störningar har vi anemi, demens genom dialys och en ökning i bensjukdomar.
referenser
- Wikipedia. (2018). Aluminiumsulfat Hämtad från: en.wikipedia.org
- Aris Industrial Aluminiumsulfatlösning typ A och B. Hämtad från: aris.com.pe
- Christopher Boyd (9 juni 2014). Topp industriella användningsområden för aluminiumsulfat. Hämtad från: chemservice.com
- PubChem. (2018). Aluminiumsulfat vattenfritt. Hämtad från: pubchem.ncbi.nlm.nih.gov
- Andesia Chemicals (20 augusti 2009). Säkerhetsblad av aluminiumsulfat. [PDF]. Hämtad från: andesia.com
- Kemisk bok. (2017). Aluminiumsulfat. Hämtad från: chemicalbook.com


