Berylliumhydroxid (Be (OH) 2) kemisk struktur, egenskaper och användningsområden
den berylliumhydroxid är en kemisk förening som består av två molekyler hydroxid (OH) och en berylliummolekyl (Be). Dess kemiska formel är Be (OH)2 och det karakteriseras för att vara en amfotär art. I allmänhet kan den erhållas från reaktionen mellan berylliummonoxid och vatten, enligt följande kemiska reaktion: BeO + H2O → Be (OH)2
Å andra sidan har denna amfotära substans en molekylär konfiguration av linjär typ. Emellertid kan olika strukturer av berylliumhydroxid erhållas: alfa- och beta-form, som ett mineral och i ångfas, beroende på vilken metod som används.
index
- 1 Kemisk struktur
- 1,1 Berylliumhydroxid alfa
- 1,2 Beta Berylliumhydroxid
- 1.3 Berylliumhydroxid i mineraler
- 1.4 Damp av berylliumhydroxid
- 2 egenskaper
- 2.1 Utseende
- 2.2 Termokemiska egenskaper
- 2.3 Löslighet
- 2.4 Risker på grund av exponering
- 3 användningsområden
- 4 Erhålla
- 4.1 Erhållande metallisk beryllium
- 5 referenser
Kemisk struktur
Denna kemiska förening kan hittas på fyra olika sätt:
Berylliumhydroxid alfa
Genom att tillsätta ett basiskt reagens, såsom natriumhydroxid (NaOH) till en berylliumsaltlösning, erhålles alfa (a) -formen av berylliumhydroxid. Ett exempel visas nedan:
2NaOH (utspädd) + BeCl2 → Be (OH)2↓ + 2NaCl
2NaOH (utspädd) + BeSO4 → Be (OH)2↓ + Na2SW4
Beryllium-beta-hydroxid
Degenerationen av denna alfa-produkt bildar en metastabil tetragonal kristallstruktur, vilken efter en lång tidsperiod har omvandlats till en rhombisk struktur som kallas berylliumhydroxid beta (P).
Denna beta-form erhålls också som en fällning från en lösning av natriumberyllium genom hydrolys under betingelser nära smältpunkten.
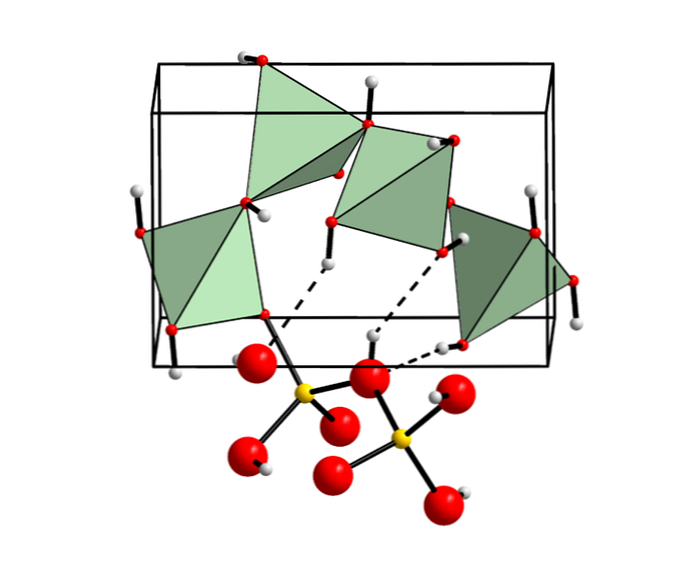
Berylliumhydroxid i mineraler
Även om det inte är vanligt, finns berylliumhydroxid som ett kristallint mineral som kallas behoite (kallas på detta sätt med hänvisning till dess kemiska sammansättning).
Det förekommer i granitiska pegmatiter som bildas av förändringen av gadolinit (mineraler av gruppen silikater) i vulkaniska fumaroler.
Detta -relativt nytt mineral upptäcktes först 1964, och finns för närvarande bara i granitpegmatiter som finns i delstaterna Texas och Utah i USA..
Ång av berylliumhydroxid
Vid temperaturer över 1200 ° C (2190 ° C) finns berylliumhydroxid i ångfasen. Den erhålles från reaktionen mellan vattenånga och berylliumoxid (BeO).
På liknande sätt har den resulterande ångan ett partiellt tryck av 73 Pa, mätt vid en temperatur av 1500 ° C.
egenskaper
Berylliumhydroxiden har en molvikt eller approximativ molekylvikt av 43,0268 g / mol och en densitet av 1,92 g / cm ^3. Dess smältpunkt ligger vid en temperatur av 1000 ° C, där den börjar sin sönderdelning.
Som ett mineral är Be (OH)2 (behoita) har en hårdhet av 4 och dens densitet varierar mellan 1,91 g / cm3 och 1,93 g / cm3.
utseende
Berylliumhydroxid är ett vitt fast ämne, som i sin alfaform har ett gelatinöst och amorft utseende. Å andra sidan utgör beta-formen av denna förening en väldefinierad, ortorhombisk och stabil kristallin struktur.
Man kan säga att morfologin hos mineralet Be (OH)2 det är varierat, eftersom det kan hittas som retikalkristaller, arborescenta eller sfäriska aggregat. På samma sätt kommer den i vitt, rosa, blåaktigt och jämnt färglöst och med en oljig glansig glans.
Termokemiska egenskaper
Entalpy av bildning: -902,5 kJ / mol
Gibbs energi: -815,0 kJ / mol
Entropi av bildning: 45,5 J / mol
Värmekapacitet: 62,1 J / mol
Specifik värmekapacitet: 1,443 J / K
Standard entalpy av bildning: -20,98 kJ / g
löslighet
Berylliumhydroxid är amfotert i sin natur, så det kan donera eller acceptera protoner och löser upp både sura och basiska medier i en syrabasreaktion som producerar salt och vatten.
I detta avseende är lösligheten hos Be (OH)2 i vatten begränsas av löslighetsprodukten Kps(H2O), vilket är lika med 6,92 × 10-22.
Exponeringsrisker
Den lagligt tillåtna exponeringsgränsen för människor (PEL eller OSHA) av en berylliumhydroxidämne definierad för en maximal koncentration mellan 0,002 mg / m3 och 0,005 mg / m3 är 8 timmar och för en koncentration av 0,0225 mg / m3 högst 30 minuter.
Dessa begränsningar beror på att beryllium är klassificerat som ett cancerframkallande typ A1 (cancerframkallande för människor, baserat på mängden av bevis från epidemiologiska studier).
tillämpningar
Användningen av berylliumhydroxid som råmaterial för bearbetning av en viss produkt är mycket begränsad (och ovanligt). Det är emellertid en förening som används som ett huvudreagens för syntesen av andra föreningar och erhållandet av berylliummetall.
erhålla
Berylliumoxid (BeO) är den kemiska föreningen av beryllium med hög renhet som används mest inom industrin. Det karakteriseras som ett färglöst fast material med egenskaper för elektrisk isolering och hög värmeledningsförmåga.
I detta avseende utförs processen för syntesen (i teknisk kvalitet) i primärindustrin på följande sätt:
- Berylliumhydroxiden löses i svavelsyra (H2SW4).
- När reaktionen utförs filtreras lösningen, så att olösliga föroreningar av oxid eller sulfat elimineras på detta sätt..
- Filtratet underkastas en indunstning för att koncentrera produkten, vilken kyles för erhållande av kristaller av berylliumsulfat BeSO4.
- BeSO4 kalcineras vid en specifik temperatur mellan 1100 ° C och 1400 ° C.
Slutprodukten (BeO) används för tillverkning av speciella keramiska bitar för industriellt bruk.
Erhållande metallisk beryllium
Under extraktion och bearbetning av berylliummineraler alstras föroreningar, såsom berylliumoxid och berylliumhydroxid. Den senare utsätts för en serie transformationer tills man erhåller det metalliska berylliumet.
Be (OH) reageras2 med en lösning av ammoniumbifluorid:
Be (OH)2 + 2 (NH4) HF2 → (NH4)2BEF4 + 2 H2O
Den (NH4)2BEF4 den utsätts för en temperaturökning, som uppvisar en termisk sönderdelning:
(NH4)2BEF4 → 2NH3 + 2HF + BeF2
Slutligen resulterar reduktionen av berylliumfluorid vid en temperatur av 1300 ° C med magnesium (Mg) i berylliummetall:
BEF2 + Mg → Be + MgF2
Beryllium används i metalllegeringar, produktion av elektroniska komponenter, tillverkning av strålningsskärmar och fönster som används i röntgenapparater.
referenser
- Wikipedia. (N.D.). Berylliumhydroxid. Hämtad från en.wikipedia.org
- Holleman, A. F .; Wiberg, E. och Wiberg, N. (2001). Berylliumhydroxid. Hämtad från books.google.co.ve
- Publicering, M. D. (s.f.). Behoite. Hämtad från handbookofmineralogy.org
- Alla reaktioner. (N.D.). Berylliumhydroxid Be (OH)2. Hämtad från allreactions.com
- PubChem. (N.D.). Berylliumhydroxid. Hämtad från pubchem.ncbi.nlm.nih.gov
- Walsh, K.A och Vidal, E.E. (2009). Berylliumkemi och -behandling. Hämtad från books.google.co.ve


