Natriumklorid (NaCl) struktur, egenskaper, användningsområden, toxicitet
den natriumklorid, även kallad vanligt salt eller bordsalt, är ett binärt oorganiskt salt av alkalimetallnatrium och halogenklorinet. Det är den största komponenten av ätbart salt och dess mineralform är känd som halit. Dess molekylformel är NaCl och beskriver det stökiometriska förhållandet av dess joner (Na+ cl-) och inte den för en diskret molekyl (Na-Cl)
Natriumklorid är ett kristallint vitt fast ämne som bildas av kombinationen av natrium, silvervit metall, som reagerar våldsamt med vatten och klorelementet, en giftig, frätande, ljusgrön gas.

I den övre bilden visas en del NaCl-kristaller. Hur är det möjligt att två element lika farliga som Na och Cl2, Kan ett ätbart salt bildas? För det första är den kemiska ekvationen för dess bildning:
2Na (s) + Cl2(g) => 2NaCl (s)
Svaret ligger i karaktären av länken i NaCl. Att vara jonisk, egenskaperna hos Na+ och Cl- de skiljer sig diagonalt från de hos deras neutrala atomer.
Natrium är ett viktigt element, men i dess jonform. Na+ är den huvudsakliga extracellulära katjonen med en koncentration av ca 140 mEq / lt, och tillsammans med dess åtföljande anjoner, Cl- och HCO3- (bikarbonat), är huvudsakligen ansvariga för värdet av osmolaritet och extracellulär volym.
Dessutom är Na+ är ansvarig för genereringen och ledningen av nervimpulser i neuronala axoner, liksom initiering av muskelkontraktion.
NaCl har använts sedan antiken för att smaka mat och för att bevara köttet på grund av dess förmåga att eliminera bakterier och förhindra förstöring.
Det är också nödvändigt för framställning av natriumhydroxid (NaOH) och molekylärt klor (Cl2) genom omsättning av NaCl med vattnet under hydrolys:
2H2O (1) + 2 NaCl (s) => 2NaOH (ac) + Cl2(g) + H2(G)
I katoden (-) ackumuleras H2 (g) och NaOH. Under tiden ackumuleras Cl vid anoden (+)2 (G). Natriumhydroxid används vid tillverkning av tvål och klor vid tillverkning av PVC-plast.
index
- 1 Struktur av natriumklorid
- 1.1 Unitary cell
- 2 egenskaper
- 2.1 Molekylformel
- 2,2 molekylvikt
- 2.3 Fysisk beskrivning
- 2,4 färg
- 2,5 smak
- 2,6 kokpunkt
- 2,7 Smältpunkt
- 2,8 Löslighet i vatten
- 2.9 Löslighet i organiska lösningsmedel
- 2,10 Densitet
- 2.11 Ångtryck
- 2.12 Stabilitet
- 2.13 Nedbrytning
- 2,14 Viskositet
- 2.15 Korrosion
- 2,16 pH
- 3 användningsområden
- 3.1 i livsmedel
- 3.2 Industriella användningsområden
- 3.3 Hemma
- 3.4 Övriga användningsområden
- 3.5 Terapeutiska användningsområden
- 4 Toxicitet
- 4.1 Förtäring
- 4.2 Irritation och fysisk kontakt
- 5 referenser
Struktur av natriumklorid
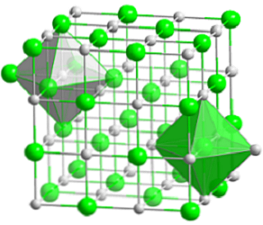
Den kompakta kubiska strukturen av natriumklorid representeras i den övre bilden. De volymgröna sfärerna motsvarar Cl anjoner-, medan vita, till Na-katjoner+. Observera hur NaCl-kristallen består av ett nätverk av joner som ordnas genom deras elektrostatiska interaktioner i ett förhållande 1: 1.
Även om staplar visas i bilden, är bindningarna inte kovalenta men joniska. Användningen av staplarna är användbar när man visar koordinationsgeometrin runt en jon. Exempelvis, i fallet med NaCl, varje Na+ är omgiven av sex Cl- (vit oktaedron) och varje Cl- av sex Na+ (grön oktaedron).
Därför har den en samordning (6,6) vars tal indikerar hur många grannar omger varje jon. Antalet till höger indikerar grannarna till Na+, medan den till vänster, Cl-.
Andra representationer släpper bort användningen av staplarna för att markera de oktaediska hålen som strukturen har, vilket är resultatet av det interstitiella utrymmet mellan sex Cl anjoner.- (eller Na-katjoner+) förpackade. Detta arrangemang observeras i andra mono (MX) eller polyatomiska oorganiska salter, och kallas pärlsalt..
Enhetlig cell
Enhetscellen i bergsaltet är kubiskt, men vilka kuber representerar exakt det i bilden ovan? Oktaedronerna ger svaret. Båda täcker totalt fyra små kuber.
Dessa kuber har delar av jonerna i sina hörn, kanter och ansikten. Observera noga, en jon Na+ Den ligger i mitten och tolv av dem i kanterna. En jon på ena kan delas av fyra kuber. Så det finns 4 Na-joner+ (12 × 1/4 + 1 = 4).
För Cl ioner-, åtta är placerade i hörnen och sex i kanterna. Eftersom jonerna placerade vid knutpunkterna delar utrymme med åtta andra kuber och vid kanterna med sex har de 4 Cl-joner- (8 × 1/8 + 6 × 1/2 = 4).
Det föregående resultatet tolkas enligt följande: i NaCl-enhetscellen finns fyra Na-katjoner+ och fyra Cl anjoner-; andel som matchar den kemiska formeln (en Na+ för varje Cl-).
egenskaper
Molekylformel
NaCl.
Molekylvikt
58,44 g / mol.
Fysisk beskrivning
En kristallin fast substans.
färg
Transparenta färglösa kristaller eller vitt kristallint pulver.
smak
salt.
Kokpunkt
2,575 ºF till 760 mmHg.
1 465 ºC.
Smältpunkt
1,474 ºF (800,7 ºC).
Både kokpunkten och smältpunkten återspeglar den värme som krävs för att övervinna den kristallina retikulära energin. Därför bekräftar dessa mätningar den joniska karaktären av NaCl.
Löslighet i vatten
Större än eller lika med 100 mg / ml vid 68 ° F.
36,0 g / 100 ml vid 25 ° C.
Det är i själva verket ett hygroskopiskt salt, som behåller fukt från miljön.
Löslighet i organiska lösningsmedel
0,065 g / 100 ml etanol vid 25 ° C; 10 g / 100 g glycerol vid 25 ° C; 2,15 g / 100 ml flytande ammonium vid 40 ° C; 1,4 g / 100 ml metanol vid 25 ° C; 7,15 g / 100 etylenglykol vid 25 ° C och 5,21 g / 100 g myrsyra vid 25 ° C.
densitet
2.165 g / cm3 vid 77 ºC.
Ångtryck
1 mmHg till 1 589 ºF.
stabilitet
Den är stabil under rekommenderade lagringsförhållanden.
sönderdelning
Vid upphettning till höga temperaturer sönderdelas utsläpp av ångor av saltsyra och dinatriumoxid.
viskositet
Viskositet av mättade lösningar 1,93 mPa s.
korrosion
Det är frätande för många metaller.
pH
6,7 till 7,3 i vattenlösning.
tillämpningar
I mat
-Natriumklorid har använts sedan antiken för att förbättra smaken av mat och dess bevarande. Saltningen av köttet är ett sätt att bevara det från bakterieverkan, eftersom det fördröjer proteinnedbrytningen.
-Å andra sidan ökar saltet osmolariteten kring köttet, vilket medför att absorptionen av osmos av bakteriens vatten orsakar eliminering.
Industriella användningsområden
Livsmedelsindustrin
-I livsmedelsindustrin används salt som en smakförstärkare, fermenteringskontrolladditiv, texturkontrollmedel och färgutvecklare. Till exempel tillsätts salt för att markera färg i bacon, skinka och andra köttprodukter.
-Salt fungerar som bindemedel vid tillverkning av korv. Det bidrar till bildandet av en bindemedelsgel som består av kött, fett och fukt.
-Vid bearbetning av mjöl för brödtillverkning tillsätts salt under kokning för att styra graden av jäsning av bröddeg. Det används också för att stärka gluten och som smakförstärkare samt fyllning av bakverk.
-Den används vid tillverkning av frukostflingor, blandade eller beredda mjöl, pommes frites, måltider för hundar och katter, etc..
Syntes av kemiska produkter
-Natriumklorid används som råmaterial vid produktion av natriumhydroxid och klor, vilket i sin tur är användbart i många kemiska industrier.
-Salt används vid bearbetning av olika metaller, till exempel aluminium, koppar, stål och vanadin. Det används också för att göra natriumklorat, som därefter användes vid syntes av klordioxid, en syrebaserad blekmedel. Klordioxid är mindre skadlig för miljön än andra blekmedel.
I läderindustrin
-Salt används för att hämma bakterieverkan inuti skinnen, samt att hjälpa till vid dess återhydrering.
I textilindustrin
-Salt används som en mordant i färgning av tyger. Den används som en saltlösning för att avlägsna organiska föroreningar och för att skapa en positiv laddning på ytan av tygerna som möjliggör förening av de negativt laddade färgerna.
I oljeindustrin
-Vid olje- och gasutforskning är salt en viktig komponent i borrvätskor. Det används för att flocka och öka tätheten hos borrvätskor, vilket gör det möjligt att övervinna gasens höga tryck i brunnarna som ska nås. Dessutom upprätthåller saltet mättnaden av borrvätskan.
-Saltet bidrar till att komprimera jorden där vägarna är byggda. Minskar förskjutningen orsakad i underjorden genom förändringar i luftfuktighet och biltrafik.
Hemma
Saltet har använts genom att gnugga i rengöring av ytor, krukor och kokkärl. Också i förebyggande av mögel och som fläckborttagare. Det används också i många märken av schampo och tandkräm.
Andra användningsområden
På vägarna
-I väntan på att snöfall vägarna är täckta med saltlösning, som förhindrar isförening till vägens yta. För upptining används en blandning av saltlösning och salt, och andra kemiska komponenter såsom magnesium eller kalciumklorider tillsätts ibland. Användningen av salt och saltlösning är inte effektiv vid temperaturer under -10ºC.
När man tillsätter salt, är det en minskning av den kryokopiska punkten, en kolligativ egenskap hos lösningarna, vilket på något sätt hindrar isbildning.
-På grund av sitt hygroskopiska tillstånd används saltet som ett billigt torkmedel.
I hartserna som används för vattenmjukning
Hårdvatten innehåller kalcium- och magnesiumjoner som hindrar verkan av tvål och producerar avlagringar av alkaliska material i olika utrustningar och rör. Vid vattenmjukning används jonbytarhartser. Salt används vid framställning och regenerering av hartser.
Brandsläckare
Natriumklorid används i brandsläckare för att bekämpa bränder där brännbara metaller är närvarande, såsom magnesium-, kalium-, natrium- och NK-legeringar.
Saltet fungerar som en kylfläns och även som en kross som begränsar syrgasens tillgång till eld.
I glasögonen
Natriumkloridkristaller används i optiska komponenter såsom fönster och prismor, speciellt för infrarött ljus. Men eftersom saltet är mycket hygroskopiskt uppstår en slags frost som täcker linserna. Av denna anledning har natriumkloridlinser ersatts med zink selenid (ZnSe).
Terapeutiska användningsområden
För att komplettera bristen på salter i kroppen
-När det finns en kroppsutarmning av Na+, måste ersättas för att upprätthålla extracellulär osmolaritet, nervledning och muskelkontraktion.
-NaCl används vid behandling och förebyggande av en brist på natrium och klor, som härrör från överdriven svettning vid exponering för höga temperaturer. Det används också vid överdriven diuresis eller överdriven begränsning av saltintaget.
-Parenteral administrering av en 045% NaCl-lösning används vid hanteringen av hyperosmolär diabetes. Det uppfyller en rehydrerande funktion och tjänar till att utvärdera statusen för njurfunktionen.
-Injektioner av hypertona lösningar, med en NaCl-koncentration som är större än 0,9% vikt / volym,
-De används när det finns en allvarlig uttömning av Na+, att vara en återställning av den väsentliga jonen. Denna hyponatremi kan vara konsekvensen av en behandling med fria elektrolyter eller med en koncentration av Na+.
Hyponatremi kan också orsakas av överdriven vattenintag, som inte kontrolleras av otillräcklig njurfunktion.
Vid behandlingar och okonventionella användningsområden
-NaCl inhalationslösningar används för att späda de läkemedel som används under nebuliseringsprocessen. Det används också för trakealtvätt och bevattning. 0,9% saltlösning som används i nässprayer.
-20% NaCl-lösningar används för intra-amniotisk transabdominal installation, vilket leder till en sen abort under graviditetens andra trimester.
-Natriumklorid kan användas som ett lokalt antiseptiskt medel. Tack vare sin osmotiska kapacitet kan den dehydrera ett brett spektrum av virus och bakterier i oförbränt tillstånd. Därför används den som en smärtsam antiseptisk för att desinficera sår.
toxicitet
intag
Det har bara en skadlig effekt på hälsan om intaget är högt och under lång tid. Under dessa omständigheter skulle hypernatremi förekomma med den därmed ökade extracellulära volymen som skulle leda till högt blodtryck.
Irritation och fysisk kontakt
Det har endast en toxisk effekt om inhalationen är mycket hög. Vid kontakt med huden i överdriven form kan det orsaka torrhet. Slutligen orsakar det en kortvarig irritation vid kontakt med ögonen.
referenser
- Shiver & Atkins. (2008). Oorganisk kemi (Fjärde upplagan, sidorna 84, 90, 93, 263). Mc Graw Hill.
- Whitten, Davis, Peck & Stanley. Kemi. (8: e upplagan). CENGAGE Learning, sid 482-483.
- Natriumklorid (2018). Natriumklorid: Fördelar, användningsområden, egenskaper, risker. Hämtad från: clorurodesodio.org
- PubChem. (2018). Natriumklorid. Hämtad från: pubchem.ncbi.nlm.nih.gov
- Wikipedia. (2018). Natriumklorid. Hämtad från: en.wikipedia.org
- Amerikanska element. (2018). Natriumklorid. Hämtad från: americanelements.com


