Hydrobromsyra (HBr) struktur, egenskaper, bildande, användningar
den Bromvätesyra är en oorganisk förening som härrör från den vattenhaltiga lösningen av en gas som kallas vätebromid. Dess kemiska formel är HBr och kan betraktas på olika sätt som motsvarar: som en molekylhydrid eller en vätehalogenid i vatten; det vill säga en hydrazid.
I kemiska ekvationer ska den skrivas som HBr (ac), för att ange att det är bromvätesyra och inte gas. Denna syra är en av de starkaste kända, ännu mer än saltsyra, HCl. Förklaringen för detta ligger i karaktären av dess kovalenta bindning.
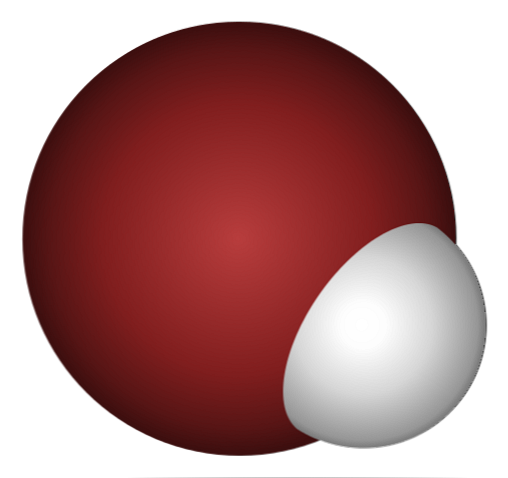
Varför är HBr en sådan syra, och ännu mer upplöst i vatten? Eftersom den kovalenta bindningen H-Br är mycket svag på grund av den dåliga överlappningen av 1s-orbitalerna av H och 4p av Br.
Detta är inte förvånande om man tittar noggrant på bilden ovan, där bromatom (klart) är klart större än vätgasen (vit).
Följaktligen orsakar någon störning uppdelningen av H-Br-bindningen, vilket frigör H-jon+. Då är bromvätesyran en Brönsted-syra, eftersom den överför protoner eller vätejoner. Dess styrka är sådan att den används vid syntesen av flera organobromerade föreningar (såsom 1-bromoetan, CH3CH2br).
Bromvätesyra är, efter hydrisk, HI, en av de starkaste och mest användbara hydrociderna för uppslutning av vissa fasta prov.
index
- 1 Struktur av bromvätesyra
- 1.1 surhet
- 2 Fysikaliska och kemiska egenskaper
- 2.1 Molekylformel
- 2,2 molekylvikt
- 2.3 Fysisk utseende
- 2.4 lukt
- 2,5 Luktgräns
- 2,6 Densitet
- 2,7 Smältpunkt
- 2,8 kokpunkt
- 2.9 Löslighet i vatten
- 2.10 Ångdensitet
- 2,11 pKa surhet
- 2.12 Kalorikapacitet
- 2.13 Standard molarenthalpi
- 2.14 Standard molar entropi
- 2,15 Flampunkt
- 3 nomenklaturen
- 4 Hur bildas det?
- 4.1 Blandning av väte och brom i vatten
- 4.2 Fosfortribromid
- 4.3 Svaveldioxid och brom
- 5 användningar
- 5.1 Framställning av bromider
- 5.2 Syntes av alkylhalogenider
- 5,3 katalysator
- 6 referenser
Struktur av bromvätesyra
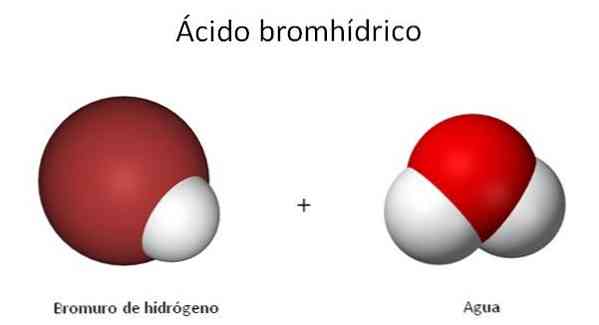
Strukturen hos H-Br visas i bilden, vars egenskaper och egenskaper, även de hos gasen, är nära besläktade med dess vattenhaltiga lösningar. Därför kommer en punkt där du kommer i förvirring om vilken av de två föreningarna som hänvisas till: HBr eller HBr (ac).
Strukturen hos HBr (ac) skiljer sig från HBr, för nu solvatiserar vattenmolekyler denna diatomiska molekyl. När den är tillräckligt nära överförs H+ till en H-molekyl2Eller som anges i följande kemiska ekvation:
HBr + H2O => Br-- + H3O+
Således består strukturen av bromvätesyran av Brjoner-- och H3O+ interagerar elektrostatiskt. Nu är det lite annorlunda än den kovalenta bindningen av H-Br.
Dess stora surhet beror på den skrymmande anjonen Br- kan knappt interagera med H3O+, kan inte hindra honom från att överföra H+ till en annan kringliggande kemisk art.
syrlighet
Exempelvis är Cl- och F- även om de inte bildar kovalenta bindningar med H3O+, de kan interagera genom andra intermolekylära krafter, såsom vätebroar (som bara F- kan acceptera dem). Vätebroarna F--H-OH2+ "Hinder" donationen av H+.
Det är av denna anledning att fluorvätesyra, HF, är en svagare syra i vatten än bromvätesyra; sedan de joniska interaktionerna Br- H3O+ stör inte överföringen av H+.
Emellertid, även om vatten är närvarande i HBr (ac), är dess beteende vid slutet av kontot liknande det för en H-Br-molekyl; det vill säga en H+ Det överförs från HBr eller Br-H3O+.
Fysikaliska och kemiska egenskaper
Molekylformel
HBr.
Molekylvikt
80 972 g / mol. Observera att, som nämnts i föregående avsnitt, anses endast HBr och inte vattenmolekylen. Om molekylvikten tas från formeln Br-H3O+ det skulle ha ett värde av 99 g / mol ungefär.
Fysiskt utseende
Färglös eller ljusgul vätska, som beror på koncentrationen av upplöst HBr. Ju mer gult det är desto mer koncentrerat och farligt blir det.
lukt
Akrid, irriterande.
Lukttröskel
6,67 mg / m3.
densitet
1,49 g / cm3 (vattenhaltig lösning vid 48% vikt / vikt). Detta värde, som de som motsvarar smältnings- och kokpunkten, beror på mängden HBr upplöst i vattnet.
Smältpunkt
-11ºC (12ºF, 393ºK) (vattenlösning vid 49% vikt / vikt).
Kokpunkt
122 ° C (252 ° F 393 ° K) vid 700 mmHg (vattenlösning 47-49% vikt / vikt).
Löslighet i vatten
-221 g / 100 ml (vid 0 ° C).
-204 g / 100 ml (15 ºC).
-130 g / 100 ml (100 ºC).
Dessa värden avser gasformig HBr, inte till bromvätesyra. Som kan ses, minskar temperaturen lösligheten hos HBr; beteende som är naturligt i gaser. Om det behövs koncentrerade HBr (ac) lösningar är det därför bättre att arbeta med dem vid låga temperaturer.
Om man arbetar vid höga temperaturer kommer HBr att fly i form av gasformiga diatomiska molekyler, så reaktorn måste förseglas för att förhindra läckage.
Ångdensitet
2,71 (i förhållande till luft = 1).
Surhet pKa
-9,0. Denna konstanta så negativa indikerar sin stora styrka av surhet.
Kalorikapacitet
29,1 kJ / mol.
Standard molarenthalpi
198,7 kJ / mol (298 ºK).
Standard molar entropi
-36,3 kJ / mol.
Tändpunkt
Ej brandfarligt.
nomenklatur
Dess namn "bromvätesyra" kombinerar två fakta: närvaron av vatten, och att brom har en valens av -1 i föreningen. På engelska är det något tydligare: bromvätesyra, där prefixet "hydro" (eller hydro) avser vatten; även om det verkligen kan referera till väte.
Brom har en valens av -1 eftersom den är bunden till väteatom mindre elektronegativ än den är; men om det är kopplat eller interagerar med syreatomer kan det ha många valenser, såsom: +2, +3, +5 och +7. Med H kan endast adoptera en enda valens, och det är därför suffixet -ico läggs till i sitt namn.
Medan HBr (g), vätebromid, är vattenfri; det vill säga det har inte vatten. Därför heter det under andra nomenklaturstandarder, som motsvarar den för vätehalogenider.
Hur bildas det?
Det finns flera syntesmetoder för framställning av bromvätesyra. Några av dem är:
Blandning av väte och brom i vatten
Utan att beskriva de tekniska detaljerna kan denna syra erhållas från den direkta blandningen av väte och brom i en reaktor fylld med vatten.
H2 + Br2 => HBr
På det sättet, som HBr bildar, löses det upp i vattnet. Detta kan dra det i destillationerna, så lösningar kan extraheras med olika koncentrationer. Vätgas är en gas och brom en mörkrödaktig vätska.
Fosfortribromid
I en mer utförd process blandas sand, hydratiserad röd fosfor och brom. Vattenfångare placeras i isbad för att förhindra att HBr flyr och bildar, istället, bromvätesyra. Reaktionerna är:
2P + 3Br2 => 2PBr3
PBr3 + 3H2O => 3HBr + H3PO3
Svaveldioxid och brom
Ett annat sätt att förbereda det är att reagera brom med svaveldioxid i vatten:
Br2 + SW2 + 2H2O => 2HBr + H2SW4
Detta är en redoxreaktion. Br2 det minskar, det tjänar elektroner, genom att länka med vätena; medan SO2 det oxiderar, det förlorar elektroner, när det bildar mer kovalenta bindningar med andra oxygener, som i svavelsyra.
tillämpningar
Framställning av bromider
Bromidsalterna kan framställas om HBr (ac) reageras med en metallhydroxid. Till exempel anses produktion av kalciumbromid:
Ca (OH)2 + 2HBr => CaBr2 + H2O
Ett annat exempel är för natriumbromid:
NaOH + HBr => NaBr + H2O
Således kan många av de oorganiska bromiderna framställas.
Syntes av alkylhalogenider
Och vad sägs om organiska bromider? Dessa är organobromerade föreningar: RBr eller ArBr.
Dehydratisering av alkoholer
Råmaterialet för att få dem kan vara alkoholer. De den protoneras av surheten i HBr och bildar vatten, som är en bra lämnande grupp, och i stället den skrymmande Br-atom, som kommer att kovalent bundet kol är införlivat:
ROH + HBr => RBr + H2O
Denna uttorkning utförs vid temperaturer över 100 ° C för att underlätta rupturen av R-OH-bindningen2+.
Tillsats till alkener och alkyner
HBr-molekylen kan tillsättas från sin vattenhaltiga lösning till dubbel- eller trippelbindningen av en alken eller alkyn:
R2C = CR2 + HBr => RHC-CRBr
RC = CR + HBr => RHC = CRBr
flera produkter kan erhållas, men under enkla förhållanden är primärt formad produkt där brom är bunden till en sekundär, tertiär eller kvaternär kolatom (Markovnikov-regeln).
Dessa halogenider ingriper i syntesen av andra organiska föreningar, och deras användningsområde är mycket omfattande. Dessutom kan några av dem även användas vid syntes eller design av nya droger.
Eterisk kliv
Från etrarna kan två alkylhalogenider erhållas samtidigt som var och en bär en av de två sidokedjorna R eller R 'i den ursprungliga etern R-O-R'. Det händer något som liknar dehydrering av alkoholer, men dess reaktionsmekanism är annorlunda.
Reaktionen kan schematiseras med följande kemiska ekvation:
ROR '+ 2HBr => RBr + R'Br
Och vatten släpps också.
katalysator
Dess surhet är sådan att den kan användas som en effektiv syrakatalysator. I stället för att lägga till Br anion- till den molekylära strukturen, öppnar vägen för en annan molekyl att göra det.
referenser
- Graham Solomons T.W., Craig B. Fryhle. (2011). Organisk kemi. Aminer. (10th upplagan.). Wiley Plus.
- Carey F. (2008). Organisk kemi (Sjätte upplagan). Mc Graw Hill.
- Steven A. Hardinger. (2017). Illustrerad ordlista för organisk kemi: bromvätesyra. Hämtad från: chem.ucla.edu
- Wikipedia. (2018). Bromvätesyra. Hämtad från: en.wikipedia.org
- PubChem. (2018). Bromvätesyra. Hämtad från: pubchem.ncbi.nlm.nih.gov
- Institutet för säkerhet och hygien på arbetsplatsen. (2011). Vätebromid [PDF]. Hämtad från: insht.es
- PrepChem. (2016). Framställning av bromvätesyra. Hämtad från: prepchem.com


