Kaliumjodoat Egenskaper, struktur, användningsområden och risker
den kaliumjodat eller kaliumjodat är en oorganisk jodförening, speciellt ett salt vars kemiska formel är KIO3. Jodelementet i gruppen av halogener (F, Cl, Br, I, As) har i detta salt ett oxidationsnummer av +5; På grund av detta är det ett starkt oxidationsmedel. KIO3 dissocieras i vattenhaltigt medium för att skapa K-jonerna+ och IO3-.
Den syntetiseras genom att reagera kaliumhydroxid med jodsyra: HIO3(aq) + KOH (s) => KIO3(aq) + H2O (l) Det kan också syntetiseras genom att reagera molekylärt jod med kaliumhydroxid: 3I2(er) + 6KOH (s) => KIO3(aq) + 5KI (aq) + 3H2O (l).

index
- 1 Fysikaliska och kemiska egenskaper
- 1.1 Oxiderande medel
- 2 Kemisk struktur
- 3 Användningar och tillämpningar av kaliumjodat
- 3.1 Terapeutisk användning
- 3.2 Användning i branschen
- 3.3 Analytisk användning
- 3.4 Användning i laserteknik
- 4 Hälsorisker av kaliumjodat
- 5 referenser
Fysikaliska och kemiska egenskaper
Det är ett luktfritt vitt fast ämne, med fina kristaller och en kristallin struktur av monoklinisk typ. Den har en densitet av 3,98 g / ml, en molekylvikt av 214 g / mol och har absorptionsband i infrarött (IR) spektrum.
Den har en smältpunkt: 833 ºK (560 ºC), i överensstämmelse med de starka joniska interaktionerna mellan K ionerna+ och IO3-. Vid högre temperaturer genomgår den en termisk sönderdelningsreaktion, som frigör molekylärt syre och kaliumjodid:
2KIO3(s) => 2KI (s) + 3O2(G)
Den har lösligheter i vatten sträcker sig från 4,74g / 100mL till 0 ° C, till 32,3 g / 100 ml till 100 ° C, som genererar färglösa vattenlösningar. Dessutom är det olösligt i alkohol och salpetersyra, men är lösligt i utspädd svavelsyra.
Dess affinitet för vatten är inte märkbar, vilket förklarar varför det inte är hygroskopiskt och existerar inte i form av hydratiserade salter (KIO)3· H2O).
Oxiderande medel
Kaliumjodat, som indikerat med sin kemiska formel, har tre syreatomer. Detta är ett starkt electronegative element och, på grund av denna egenskap, "det avslöjar" en elektronisk brist i molnet som omger jod.
Denna brist, eller inmatning, som fall- kan beräknas som antalet oxidation av jod (± 1, 2, 3, 5, 7), som är 5 i fallet med detta salt.
Vad betyder detta? Att före en art som kan ge sina elektroner, accepterar jod dem i deras jonform (IO3-) för att bli molekylärt jod och ha ett oxidationsnummer lika med 0.
Efter denna förklaring kan det bestämmas att kaliumjodat är en oxidationsförening som reagerar starkt med reduktionsmedel i många redoxreaktioner; av alla dessa är en känd som jodklockan.
Jodklockan består av en redox-process med långsamma och snabba steg, där de snabba stegen markeras med en KIO-lösning3 i svavelsyra, till vilken stärkelse tillsättes. Därefter stärkelsen - en gång framställd och förankrad mellan dess strukturart I3-- kommer att vända lösningen från färglös till mörkblå.
IO3- + 3 HSO3- → I- + 3 HSO4-
IO3- + 5 I- + 6 H+ → 3 I2 + 3 H2O
jag2 + HSO3- + H2O → 2 I- + HSO4- + 2 H+ (mörkblå på grund av stärkelseffekten)
Kemisk struktur
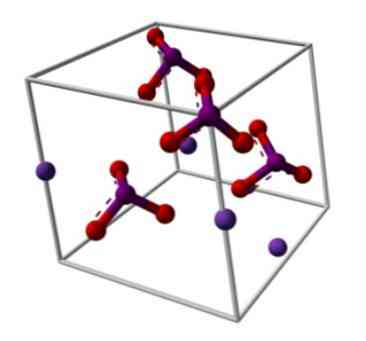
Kemisk struktur av kaliumjodat illustreras i den övre bilden. IO-anjonen3- representeras av "stativet" av röda och lila sfärer, medan K-jonerna+ De representeras av de lila sfärerna.
Men vad betyder dessa stativ? De korrekta geometriska former av dessa anjoner är faktiskt trigonal pyramider, i vilka syreatomerna bildar den triangulära basen, och odelat elektronpar jod pekar uppåt, som upptar utrymme och tvingar vika ner IO länken och de två länkar I = O.
Denna molekylära geometri motsvarar en sp-hybridisering3 av den centrala jodatomen; emellertid antyder ett annat perspektiv att en av syreatomerna bildar bindningar med jodens "d" orbitaler, i själva verket är en sp hybridisering3d2 (jodet kan ha sina "d" orbitaler som utökar sitt valensskal).
Kristallerna i detta salt kan genomgå övergångar av strukturfas (andra arrangemang än monokliniska) som en följd av de olika fysiska förhållandena som utsätter dem.
Användningar och användningar av kaliumjodat
Terapeutisk användning
Kaliumjodat används vanligtvis för att förhindra ackumulering av radioaktivitet i sköldkörteln i form av 131Jag, när denna isotop används vid bestämning av jodupptaget av sköldkörteln som en del av sköldkörtelns funktion.
På samma sätt används kaliumjodat som en topisk antiseptisk (0,5%) i slemhinnaninfektioner.
Användning i branschen
Det läggs till djurfoderens utfodring som ett jodtillskott. Därför används kaliumjodat i industrin för att förbättra mjölkens kvalitet.
Analytisk användning
I analytisk kemi, tack vare dess stabilitet, används den som en primär standard vid standardisering av natriumtiosulfat standardlösningar (Na2S2O3) för att bestämma jodkoncentrationerna i proverna.
Detta innebär att mängderna jod kan vara kända genom volymetriska tekniker (titreringar). I denna reaktion oxiderar kaliumjodat snabbt jodidjoner I-, med följande kemiska ekvation:
IO3- + 5I- + 6H+ => 3I2 + 3H2O
Jod, jag2, har titeln med lösningen av Na2S2O3 för dess standardisering.
Används i laserteknik
Studier har visat och bekräftat de intressanta piezoelektriska, pyroelektriska, elektrooptiska, ferroelektriska egenskaperna och i den icke-linjära optiken av KIO-kristaller3. Detta resulterar i stor potential inom elektronikområdet och i laserns teknik för material gjorda med denna förening.
Hälsorisker av kaliumjodat
Vid höga doser kan det orsaka irritation i munslimhinnan, huden, ögonen och andningsorganen.
Experiment av toxiciteten av kaliumjodat i djur har tillåtit att observera att i fastande hundar i doser från 0,2 till 0,25 g / kg kroppsvikt, föredraget oralt, det orsakar kräkningar förening.
Om dessa kräkningar undviks, orsakar det en försämring av situationen i djuren, eftersom den inducerar anorexi och utmattning före döden. Hans obduktioner tillåts att observera nekrotiska skador i lever, njurar och tarmslimhinnor.
På grund av dess oxiderande effekt utgör den en brandrisk vid kontakt med brandfarliga material.
referenser
- Day, R., & Underwood, A. Kvantitativ analytisk kemi (femte red.). PEARSON Prentice Hall, p-364.
- Muth, D. (2008). Lasrar. [Figur]. Hämtad från: flickr.com
- ChemicalBook. (2017). Kaliumjodat. Hämtat 25 mars 2018 från ChemicalBook: chemicalbook.com
- PubChem. (2018). Kaliumjodat. Hämtat 25 mars 2018, från PubChem: pubchem.ncbi.nlm.nih.gov
- Merck. (2018). Kaliumjodat. Hämtat den 25 mars 2018, från Merck:
- merckmillipore.com
- Wikipedia. (2017). Kaliumjodat. Hämtad den 25 mars 2018, från Wikipedia: en.wikipedia.org
- M M Abdel Kader et al. (2013). Laddningstransportmekanism och lågtemperaturfasövergångar i KIO3. J. Phys.: Conf. Ser. 423 012036


