Butino struktur, egenskaper och användningsområden
den butyn är en kemisk förening som tillhör gruppen alkyner, karakteriseras huvudsakligen genom att ha i sin struktur åtminstone en trippelbindning mellan två kolatomer.
När det gäller att fastställa regler för namngivning alkyner, IUPAC (står för International Union of Pure and Applied Chemistry) har fastslagit att de används som för alkener.

Den grundläggande skillnaden mellan nomenklaturen för båda typerna av ämnen är att suffixet -one ändras till -eller när det gäller föreningar som har tredubbla bindningar i sin struktur.
Å andra sidan, butyn består enbart av kol och väte, och finns i två former: 1-butyn, som är i gasfas under betingelser av standardtemperatur och -tryck (1 atm, 25 ° C); och 2-butino, som är en flytande fasart framställd genom kemisk syntes.
index
- 1 Kemisk struktur
- 1,1 1-butino
- 1,2 2-butyn
- 2 egenskaper
- 3 användningsområden
- 4 referenser
Kemisk struktur
I butyn molekyl känd som fenomenet med strukturell isomerism av position, vilket är närvaron av dessa funktionella grupper i båda föreningarna, men var och en av dessa är på en plats annan än kedjan inträffar.
I detta fall har båda formerna av butino en identisk molekylformel; I 1-butyn är den tredubbla bindningen emellertid i kol nummer 1, medan den i 2-butyn finns i nummer två. Detta omvandlar dem till positionsisomerer.
På grund av placeringen av trippelbindningen i en av terminalerna av strukturen av en-butyn, betraktas det som en terminal alkyn, medan den mellersta positionen av trippelbindningen i strukturen av 2-butyn ger klassificeringen interna alkynen.
Således kan länken endast vara mellan det första och andra kolet (1-butyn) eller mellan det andra och tredje kolet (2-butyn). Detta beror på den tillämpade nomenklaturen, där den lägsta möjliga numreringen alltid kommer att ges till triple bond-positionen.
1-butyn
Föreningen som kallas 1-butyn är också känd som etylacetylen, på grund av dess struktur och sättet på vilket dess fyra kolatomer är anordnade och bundna. Men när man pratar om butyn Det hänvisas endast till denna kemiska art.
I denna molekyl finns den tredubbla bindningen i ett terminal kol, vilket möjliggör tillgängligheten av väteatomer som ger den stor reaktivitet.
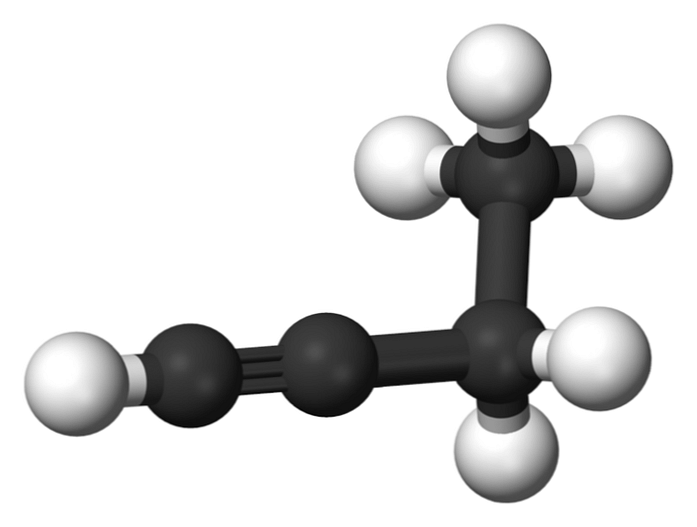
Denna styva och starkare bindning än en enkel- eller dubbelbindning mellan kolatomerna ger en stabil konfiguration av 1-butynlinjär geometri.
Å andra sidan är detta gasformiga ämne ganska brandfarligt, så i närvaro av värme kan det lätt orsaka bränder eller explosioner och har stor reaktivitet i närvaro av luft eller vatten.
2-butyn
Eftersom inre alkyner uppvisar större stabilitet än terminala alkyner tillåter de omvandlingen av 1-butyn till 2-butyn.
Denna isomerisering kan ske genom upphettning av en-butyn i närvaro av en bas (såsom NaOH, KOH, NaOCH3 ...) eller genom införlivande av 1-butyn i en lösning av kaliumhydroxid (KOH) i etanol (C2H6O).
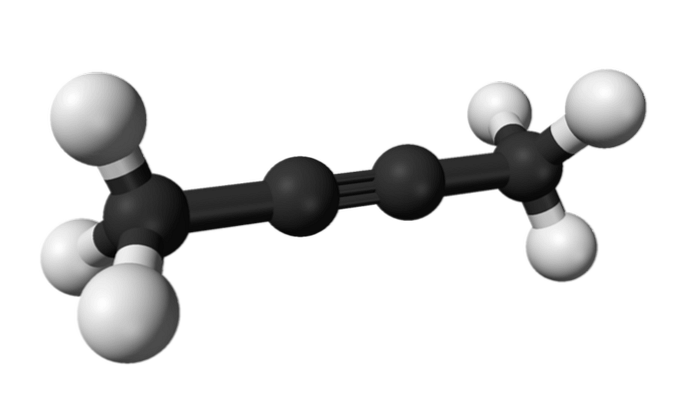
På samma sätt kallas kemikalien som kallas 2-butyn också dimetylacetylen (eller krotonylen), som presenterar sig som en flytande och flyktig art som härstammar artificiellt.
I 2-butyn är den tredubbla bindningen i mitten av molekylen, vilket ger den större stabilitet än dess isomer.
Dessutom har denna färglösa förening en lägre densitet än vatten även om den anses vara olöslig i den och har en hög brandfarlighet.
egenskaper
-Strukturformeln för butino (oavsett vilken isomer som refereras) är C4H6, som har en linjär struktur.
-En av de kemiska reaktioner som uppstår av butinmolekylen är isomerisering, där en omplacering och migrering av trippelbindningen sker inom molekylen.
-1-Butyn är i gasfas, har en mycket hög brandfarlighet och högre densitet än luft.
-Detta ämne är också ganska reaktivt, och i närvaro av värme kan det orsaka våldsamma explosioner.
-Dessutom, när denna färglösa gas upplever en ofullständig förbränningsreaktion kan det orsaka kolmonoxid (CO)
-När båda isomerer utsätts för höga temperaturer kan de uppleva polymeriseringsreaktioner av explosiv typ.
-2-butyn är i vätskefasen, även om den också anses vara ganska brandfarlig under normala tryck- och temperaturförhållanden.
-Dessa ämnen kan uppleva våldsamma reaktioner när de är i närvaro av starka oxiderande ämnen.
-På samma sätt uppträder exoterma reaktioner med en följdfri frigöring av gasformigt väte när de är i närvaro av reducerande arter..
-När det finns kontakt med vissa katalysatorer (såsom vissa sura substanser) eller startarter kan exoterma polymerisationsreaktioner förekomma.
tillämpningar
Eftersom de har olika egenskaper, kan båda isomerer ha olika användningsområden och applikationer, som visas nedan:
För det första är en av applikationerna av 1-butino ofta använd som ett mellanstadium i produktionsprocessen av andra ämnen av organisk art av syntetiskt ursprung..
Å andra sidan används denna kemiska art i tillverkningsindustrin av gummi och härledda föreningar; som till exempel när du vill få bensol.
På samma sätt används den i tillverkningsprocessen av en mängd olika plastprodukter, liksom vid framställning av många polyetenämnen betraktad som hög densitet.
Dessutom används 1-butyn ofta som en komponent för skärnings- och svetsprocesser av vissa metalllegeringar, inklusive stål (järnlegering och kol)..
I en annan mening är isomeren 2-butyn används i kombination med en annan namngiven alkyn propyn i syntesen av vissa substanser som är kända som alkylerade hydrokinoner, när processen för syntes av α-Total tokoferol (vitamin E) utförs.
referenser
- Wikipedia. (N.D.). Butyn. Hämtad från en.wikipedia.org
- Yoder, C.H., Leber P.A. och Thomsen, M.W. (2010). Broen till organisk kemi: Begrepp och nomenklatur. Hämtad från books.google.co.ve
- Study.com. (N.D.). Butyne: strukturformel och isomerer. Erhållen från studie.
- PubChem. (N.D.). 1-butyn. Hämtad från pubchem.ncbi.nlm.nih.gov
- PubChem. (N.D.). 2-butyn. Hämtad från pubchem.ncbi.nlm.nih.gov


